[ad_1]
3章 HPVワクチンによるHPV関連がんの1次予防
3.1 HPVワクチン
① 子宮頸がんおよびその他のHPV関連がんの1次予防
生活習慣や生活環境の改善、ワクチン接種などにより疾病の発生を未然に防ぐことを1次予防という。子宮頸がんは子宮頸部でのヒトパピローマウイルス(human papillomavirus:HPV)の持続的な感染が最大の原因であり、HPVの感染予防が最も重要な1次予防法となる1,2)。子宮頸がん以外にもHPV感染に起因するがんがあり(1.2参照)、これらのがんにおいてもHPVの感染予防が重要である。HPVの感染予防法には、HPVワクチン接種、子宮頸がんおよびその他のHPV関連がんのリスク因子に関する教育、安全な性行動習慣への教育と避妊具の適切な使用の推進がある。
HPVワクチン接種は、HPV感染を予防することで子宮頸がんおよび前がん病変の罹患を減少させることを目的に、2007年前後から西ヨーロッパ、オーストラリアなどで導入され、2022年11月時点で124か国において国家プログラムとして実施されている3)(3.5参照)。国立がん研究センターの「日本人のためのがん予防法」研究班は、日本人を対象としたHPVと子宮頸がんの研究の結果に基づき、HPVワクチンが子宮頸がんのリスクを低下させることについて、最も科学的根拠が強い「確実」と評価しており4)、日本も国家プログラムとしてHPVワクチンの定期接種を実施している。
② HPVワクチンが感染を予防する仕組み
ワクチンを接種するとヒトの体内で免疫応答が起こり、抗体(病気の原因となるウイルスや細菌などを攻撃したり体外に排除したりするために作られるタンパク質)を産生することで病原体の感染や感染後の発症を阻止することができる。HPVワクチンも同様で、HPVが接着して侵入する膣や子宮頸部などの粘膜や皮膚からHPVに特異的な抗体が漏れ出ることでHPVを阻止し、HPV感染を防ぐことができる。さらに、ワクチン接種が普及することにより免疫を持つ人の割合が増え、感染者が出てもほかの人に伝播しにくくなり、感染症が流行しにくくなる。この状態を集団免疫と言い、免疫を持たない人を含めて社会全体が感染症から守られることになる。
HPVには様々な遺伝子型があり、原則的に特定の型のHPV感染を同じ型の抗体で予防することになる。例えば、HPV16型に対する抗体を体内で産生させることで、HPV16型の感染を防ぐことができる。体内で抗体を産生して性器の粘膜や皮膚に抗体を出すためには、HPVワクチンを筋肉注射するのが最も有効であることがわかっている5)。血中の抗HPV抗体価は、ワクチン接種後長期間にわたり、自然感染時以上のレベルで維持されることが分かっている2)(3.2参照)。
なお、ワクチンは感染予防を目的としていて、既に感染している者からウイルスを排除する効果はなく、HPV感染症や子宮頸がんなどのHPV関連疾患を治療するものでもない。HPVは性交渉を介して感染することから、効果的な感染予防のためには、性交渉開始前にワクチンを接種することが重要である2)。
③ HPVワクチンの種類
2022年11月時点で、世界で使用されているHPVワクチンは2価(16・18型)、4価(6・11・16・18型)、9価(6・11・16・18・31・33・45・52・58型)があり、いずれも組み換えDNA技術を用いてHPVの蛋白質を発現させ、ウイルス様粒子に再構成したものを抗原として用いている。このウイルス様粒子にはDNAは含まれていないので、ワクチンに感染性はない。
国内で承認されているHPVワクチンは、2価HPVワクチン(サーバリックス)、4価HPVワクチン(ガーダシル)、9価HPVワクチン(シルガード9)の3種類がある。その内2022年11月時点で定期接種が認められているのは2価と4価HPVワクチンのみである。9価HPVワクチンは2020年7月に厚生労働省より製造販売が承認され、2021年2月より販売されているが、9歳以上の女性のみの任意接種と定められている。男性への接種は、2020年12月に4価ワクチンが9歳以上で承認されている(2022年11月時点)。9価HPVワクチンは世界保健機関(World Health Organization:WHO)でもその安全性と有効性が認められており、子宮頸がんの原因となる多くのHPV型を網羅するため、普及すれば子宮頸がんの90%あるいはそれ以上が予防可能になると期待されている(1.1参照)。
日本のワクチン政策の枠組みを検討する厚生科学審議会予防接種・ワクチン分科会予防接種基本方針部会では、2022年9月22日のワクチン評価に関する小委員会において「9価HPVワクチンの定期接種化に係る技術的な課題についての議論のとりまとめについて」をとりまとめ6)、2022年11月8日第50回厚生科学審議会予防接種・ワクチン分科会予防接種基本方針部会において、2023年4月より定期接種に用いることが了承された7)。男性への接種については、2022年8月4日のワクチン評価に関する小委員会において、定期接種化を検討していくことが提案されている8)。
④ HPVワクチンの接種対象とスケジュール
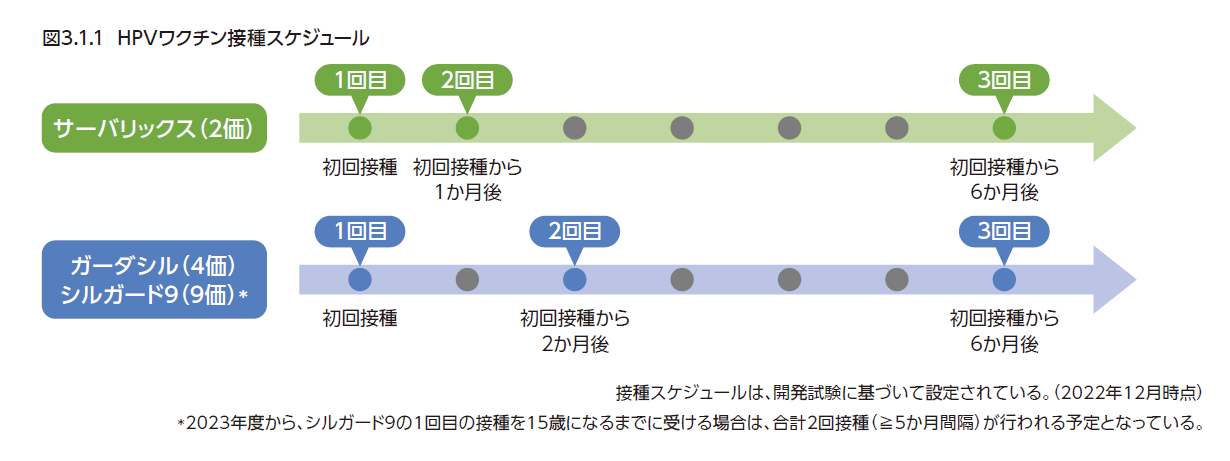
日本ではHPVワクチンの定期接種は、以下の対象とスケジュールで3回接種することが標準となっている9)(図3.1.1)。
対象:小学校6年生~高校1年生相当(おおむね12歳~16歳)の女性
- 2価ワクチン(サーバリックス):1回目の接種から1か月の間隔をおいて2回目の接種を行った後、1回目の接種から6か月の間隔をおいて3回目の接種を行う(このスケジュールで接種できない場合、2回目は1回目から1か月以上、3回目は1回目から5か月以上、2回目から2か月半以上あける)。
- 4価ワクチン(ガーダシル):1回目の接種から2か月の間隔をおいて2回目接種を行った後、1回目の接種から6か月の間隔をおいて3回目の接種を行う(このスケジュールで接種できない場合、2回目は1回目から1か月以上、3回目は2回目から3か月以上あける)。
いずれのワクチンも、1年以内に接種を終えることが望ましいとされている。なお、9価ワクチン(シルガード9)については、2022年11月現在、任意接種として接種が行われているが、2023年4月からは定期接種の対象となる。
なお、WHOは2022年12月のポジションペーパーで、免疫不全がない限りは1回あるいは2回接種を推奨しており10)、現在多くの国が9価ワクチンの2回接種を実施している2,3)(3.5参照)。日本においても2023年3月7日の厚生科学審議会予防接種・ワクチン分科会で、9価ワクチンの2回接種(≧5か月間隔)が了承され11)、2023年度から、15歳になるまでに9価ワクチンの1回目の接種を受ける場合、合計2回接種が行われる予定となっている。
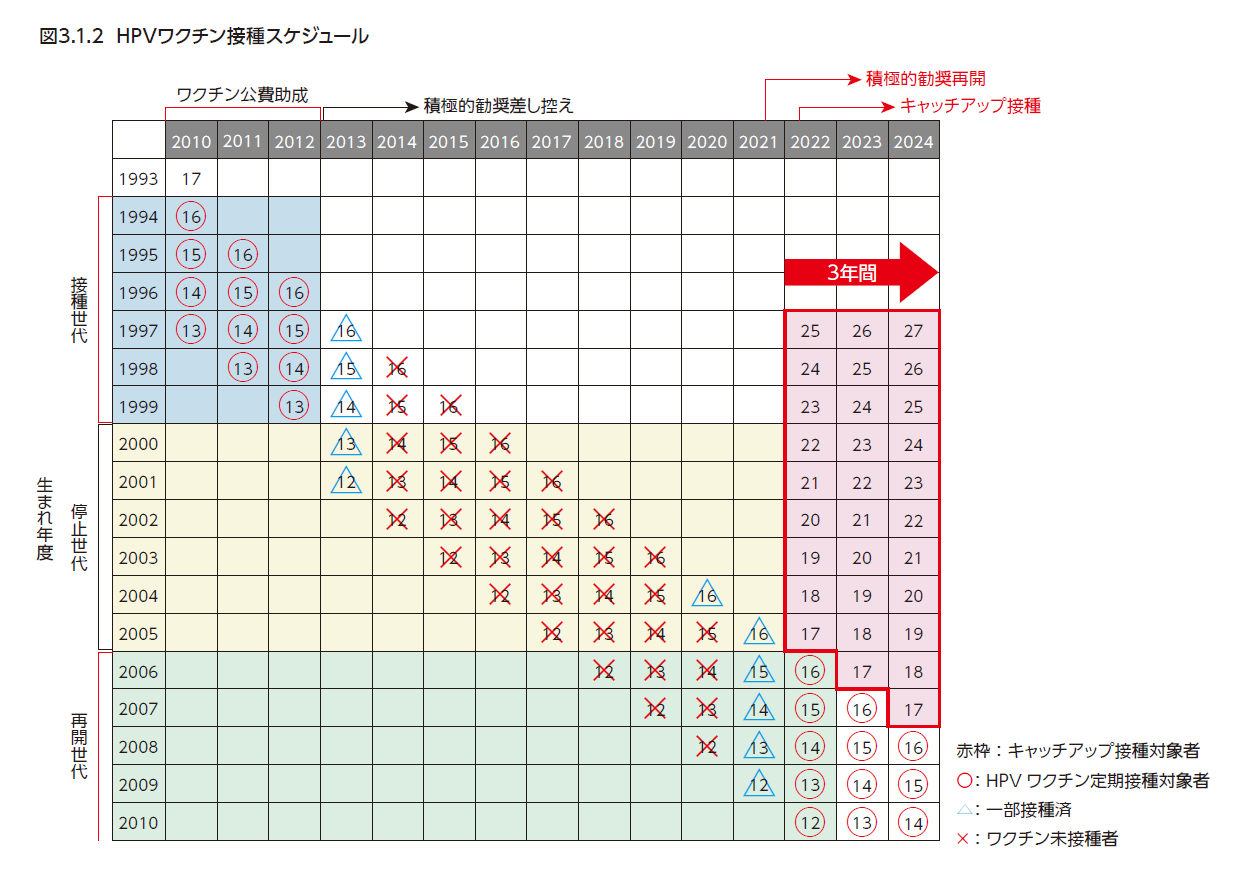
上記の対象に加え、HPVワクチン接種の積極的勧奨が差し控えられていた2013年~2021年に公費でのHPVワクチン接種の機会を逃した1997年度生まれ~2005年度生まれ(誕生日が1997年4月2日~2006年4月1日)の女性に対して、2022年4月から2025年3月末まで定期接種の対象年齢を超えて公費でのHPVワクチン接種が提供されている(キャッチアップ接種)(図3.1.2)12)。2006年度および2007年度生まれの女性についても、通常の対象年齢を超えて2025年3月末までHPVワクチン接種を受けることができる。
なお、8年以上の接種間隔が空いた場合の影響に関するエビデンスは国内外で認められていないが、海外の研究において、1年~5年の接種間隔が空いた場合、通常の接種スケジュールと比較して一定程度の免疫原性と安全性が示されている13)。諸外国においては、接種間隔が長期にわたる場合、接種間隔に上限を設けず、また接種を最初からやり直すことなく残りの回数の接種を行うこととされている。さらに、過去に接種したワクチンの種類が不明で、医療機関や自治体などからどのワクチンを接種したかの情報が得られない場合も考えられる。この場合、以前と異なる種類のワクチンを接種する交互接種を行うことになるが、現状入手可能なエビデンスによれば、2価ワクチンと4価ワクチンの交互接種について、同一のワクチンを使用した場合と比較して、一定程度の免疫原性と安全性が示されている13)。WHOのポジションペーパーによると、以前に接種した種類のワクチンが入手できない場合、あるいは不明な場合について、ほかの種類のHPVワクチンで接種を完了することが可能とされている10)。
引用文献
1)厚生労働省.「ヒトパピローマウイルスと子宮頸がんワクチン(ファクトシート)」(WHO Fact sheet日本語訳).2016年6月.
https://www.forth.go.jp/moreinfo/topics/2016/06081122.html,
(2022年11月7日アクセス)
2)国立感染症研究所.9価ヒトパピローマウイルス(HPV)ワクチンファクトシート.2021年1月31日.
https://www.mhlw.go.jp/content/10900000/001014059.pdf,
(2022年11月7日アクセス)
3)World Health Organization.「HPV vaccine included in national immunization programme」.
https://app.powerbi.com/view?r=eyJrIjoiNDIxZTFkZGUtMDQ1Ny00MDZkLThiZDktYWFlYTdkOGU2NDcwIiwidCI6ImY2MTBjMGI3LWJkMjQtNGIzOS04MTBiLTNkYzI4MGFmYjU5MCIsImMiOjh9,
(2022年11月24日アクセス)
4)国立がん研究センター.「科学的根拠に基づくがんリスク評価とがん予防ガイドライン提言に関する研究」.
https://epi.ncc.go.jp/can_prev/,
(2022年11月7日アクセス)
5)日本産婦人科学会.「子宮頸がんとHPVワクチンに関する正しい理解のために」.
https://www.jsog.or.jp/modules/jsogpolicy/index.php?content_id=4,
(2022年11月7日アクセス)
6)厚生労働省.9価HPVワクチンの定期接種化に係る技術的な課題についての議論のとりまとめについて.2022年9月20日.
https://www.mhlw.go.jp/content/10906000/000992367.pdf,
(2022年11月7日アクセス)
7)厚生労働省.「9価ヒトパピローマウイルス(HPV)ワクチン(シルガード9)について」.
https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/kenkou/hpv_9-valentHPVvaccine.html,
(2022年11月7日アクセス)
8)厚生労働省.「第19回厚生科学審議会予防接種・ワクチン分科会予防接種基本方針部会ワクチン評価に関する小委員会」.2022年8月4日.
https://www.mhlw.go.jp/stf/newpage_27566.html,
(2022年11月7日アクセス)
9)厚生労働省.「ヒトパピローマウイルス感染症~子宮頸がん(子宮けいがん)とHPVワクチン~」.
https://www.mhlw.go.jp/bunya/kenkou/kekkaku-kansenshou28/index.html,
(2022年11月7日アクセス)
10)World Health Organization. Human papillomavirus vaccines: WHO position paper, December 2022. Weekly Epidemiological Record No 50, 2022, 97, 645–672.
https://www.who.int/teams/immunization-vaccines-and-biologicals/diseases/human-papillomavirus-vaccines-(HPV),
(2023年2月6日アクセス)
11)厚生労働省.第45回厚生科学審議会予防接種・ワクチン分科会 2023年3月7日.
https://www.mhlw.go.jp/stf/newpage_31559.html,
(2023年3月23日アクセス)
12)厚生労働省.「ヒトパピローマウイルス(HPV)ワクチンの接種を逃した方へ~キャッチアップ接種のご案内~」.
https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/kenkou/hpv_catch-up-vaccination.html,
(2022年11月7日アクセス)
13)厚生労働省.第47回厚生科学審議会予防接種・ワクチン分科会予防接種基本方針部会(資料1)HPVワクチンについて.2022年1月27日.
https://www.mhlw.go.jp/content/10601000/000890273.pdf,
(2023年2月6日アクセス)
3.2 HPVワクチンによるHPV関連がん予防の有効性と安全性
3.2.1 HPVワクチンによる感染予防効果
ワクチンの臨床的予防効果は、一般的に、感染予防効果、発症予防効果、重症化予防効果に分けられ、いずれも「有効率」という指標で表されることが多い。ワクチン有効率90%とは、感染予防効果の場合、「接種なし」の者の感染率と比較して、「接種あり」の者の感染率が10分の1に減少することを示す。例えば、「接種なし」と「接種あり」のそれぞれの集団における感染率が、50%と5%、10%と1%の場合、ワクチン有効率が90%になる(相対リスクで表す場合は0.1に相当する)。いいかえると、「接種せずに感染した者のうち、90%は、接種していれば感染しなかった」ことを意味する。ワクチン間の比較の場合、「接種なし」と「接種あり」の比較ではなく、「ワクチンAの接種」と「ワクチンBの接種」を比較して有効率を計算することもある。ワクチン接種後の抗体価は、その抗体が病原体を中和(生物学的な影響を無力化)する能力を有する場合、臨床的効果の代替指標となりうる。
① 子宮頸部のHPV感染予防効果
HPVワクチン接種により、HPV感染を予防することができる。2価または4価HPVワクチンの第II相あるいは第Ⅲ相臨床試験(それぞれの追跡期間は最長で9年と6年)のメタアナリシスによると(計26試験、約74,000人)、HPV16、18型に未感染の15歳~26歳の女性(約23,000人)では、HPV16、18型の持続感染(6か月間隔で同じ型のHPVDNAが検出)に対する相対リスクは、プラセボ投与群と比較してワクチン投与群で0.10(95%信頼区間:0.08~0.12)であった。24歳~45歳の女性(約7,500人)に限った場合の相対リスクは0.17(95%信頼区間:0.10~0.29)であった。ワクチン有効率に換算するとそれぞれ90%と83%であり、いずれも高い予防効果が認められた1,2)。9価HPVワクチンについては、日本を含めた18か国105施設で、16歳~26歳の健康女性(14,215人)を対象に、4価HPVワクチンを比較対照としたランダム化二重盲検試験が行われている。9価HPVワクチンで追加された5つのHPV型(HPV31, 33, 45, 52, 58型)に対する有効率は、6か月間の持続感染に対して96.0%(95%信頼区間:94.6~97.1)、12か月の持続感染に対して96.7%(95%信頼区間:95.1~97.9)であった1,3)。同試験では、日本人女性集団(16歳~26歳、254人)のサブグループ解析も行なわれている。HPV31、33、45、52、58型の6か月以上の持続感染に対する9価HPVワクチン接種の有効率は90.4%(95%信頼区間62.4~98.4)であり、アジアのほかの国・地域(香港、台湾、韓国、タイ)と比較して有意な差は認められなかった1,4)。
日本の新潟県で、子宮頸がん検診受診者1,814人を対象に、2価HPVワクチン接種によるHPV感染の減少効果を検討した研究では、HPV16、18型の感染率は、HPVワクチン接種者(1,355人)で0.2%、非接種者(459人)で2.2%であり、有効率は89.8%(95%信頼区間:63.9~97.2)であった。初交前にワクチンを接種した者に限定したところ、HPV16、18型の感染率は、接種者(1,000人)で0.1%、非接種者(454人)で2.2%であり、有効率は95.5%(95%信頼区間:64.6~99.4)とさらに高くなった。有効率の最終数値として、性交渉パートナー数と生まれ年で補正した93.9%(95%信頼区間:44.8~99.3)が示されている1,5)。
HPVワクチン接種による交差免疫(ワクチンに含まれる抗原だけでなく、類似性の高いほかの抗原に対しても免疫を示すこと)については、ランダム化比較試験の長期追跡の結果から、2価HPVワクチン接種後4年の時点で、HPV31、33、45、51、52型の持続感染に対する一定程度の予防効果(有効率15%~80%)が報告されている1,6,7)。上述した日本の新潟県での研究では、2価HPVワクチン接種によりHPV31、45、52型の感染に対する予防効果も示された(有効率:67.7%、95%信頼区間:24.9~86.1)5)。
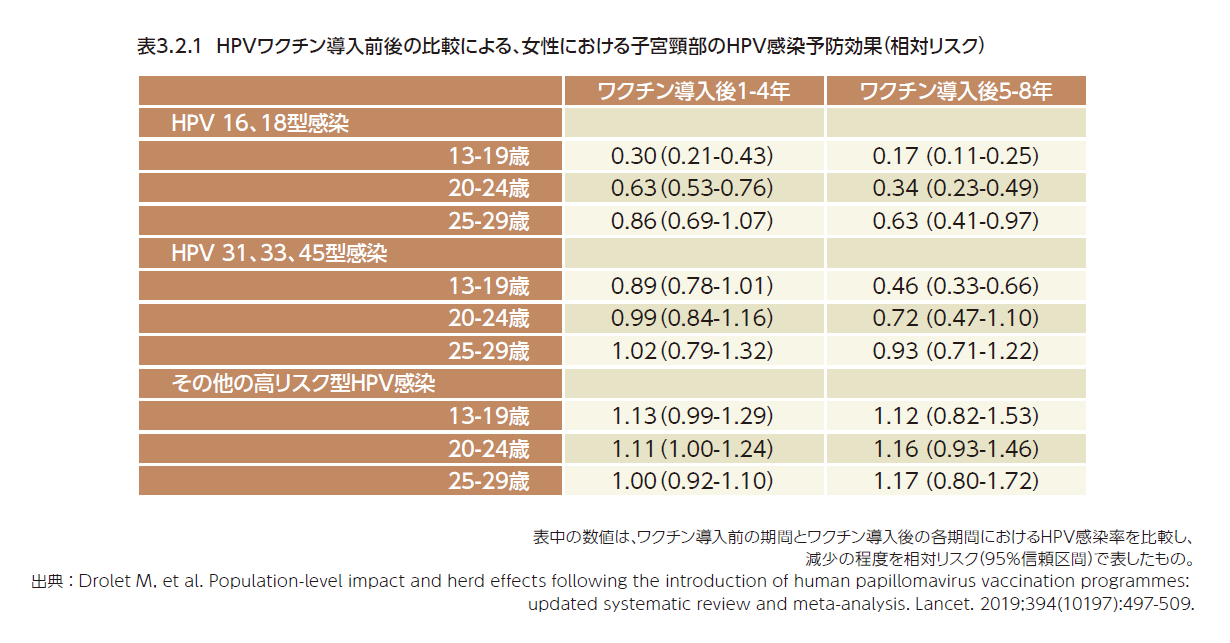
HPVワクチン接種を国家プログラムとして実施している欧米諸国で、ワクチン導入前後の比較による感染予防効果が評価されるとともに、これらの報告の大規模なメタアナリシスも行われている1,8)。2014年2月1日から2018年10月11日の期間に公表された23論文(13研究)のメタアナリシスの結果、HPV16、18型感染に対して最も顕著な効果が認められたのは13歳~19歳の女性であり、ワクチン導入前と比べて、ワクチン導入後5年~8年の時点で83%の減少が示された(表3.2.1)。高い年齢層では予防効果が低下する傾向を認め、すでにHPV16、18型に感染していることの影響を示唆している。HPV31、33、45型による感染に対しては、ワクチン導入前と比べて、ワクチン導入後5年~8年の時点で、13歳~19歳の女性で54%の予防効果が示され、交差免疫による効果と考えられる。一方で、ワクチンに含まれない高リスク型HPV全体に対しては、有意な感染予防効果が認められなかったことから、交差免疫による全体としての効果は限定的である。
日本でも、秋田県において、HPVワクチン導入前後の比較による感染予防効果が報告されている。18歳~24歳の女性におけるHPV16、18型感染率は、ワクチン導入前の群(1984年~1994年生まれ、49人)での36.7%から、ワクチン導入後の群(1989年~1999年生まれ、52人)で5.8%に低下していた1,9)。この地域での18歳~24歳女性のワクチン接種率が68.2%(2,511/3,684人)と高いことが、顕著なワクチン効果に寄与していると考えられる。
HPVワクチンによる感染予防効果の持続期間は、2価ワクチンで最大11年間、4価ワクチンで少なくとも10年間、9価ワクチンで少なくとも6年間と報告されており、現在実施中の研究から、より長期の追跡結果が待たれる10)。なお、数理モデルによって、2価ワクチン接種後少なくとも30年~50年は、自然感染時以上の抗体価が維持されることが予測されているが、HPV感染予防に必要な抗体価については不明である1)。
2価あるいは4価ワクチンと9価ワクチンの互換性(例:2価あるいは4価ワクチンを3回接種した場合と、2価あるいは4価ワクチンを2回接種後に9価ワクチンを3回目として接種した場合、同等の効果が得られるか)についての報告はほとんどない。なお、米国の予防接種諮問委員会は、過去に接種したHPVワクチンの種類が分からない場合、過去に接種したHPVワクチンが現在利用できない場合、あるいは、9価ワクチンへの移行が進んでいる状況では、その時点で入手可能な製剤を使用して、所定の接種回数を完了することを推奨している11)。
② 子宮頸部以外の部位に発生するHPV感染の予防効果
2008年~2009年にフィンランドの33地域で行われたランダム化比較試験では、出生年が1994年~1995年の青少年を対象に、2価HPVワクチン接種による中咽頭のHPV感染予防効果を評価した。18.5歳時(登録後3年~6年)の追跡調査に参加し、中咽頭の試料からHPV DNAを測定した女性 4,871人の情報を分析した結果、HPV16/18型、HPV31/45型、HPV31/33/45型の感染に対するワクチン有効率はそれぞれ82.4%(95%信頼区間: 47.3~94.1)、75.3%(12.7~93.0)、69.9%(29.6~87.1)であった12)。HPVワクチン接種による口腔や中咽頭のHPV感染予防について、2016年1月~2021年3月の期間に公表された論文を系統的レビューした結果によると、ワクチン有効率はおおむね83%前後であり、いずれも統計的に有意であった13)。
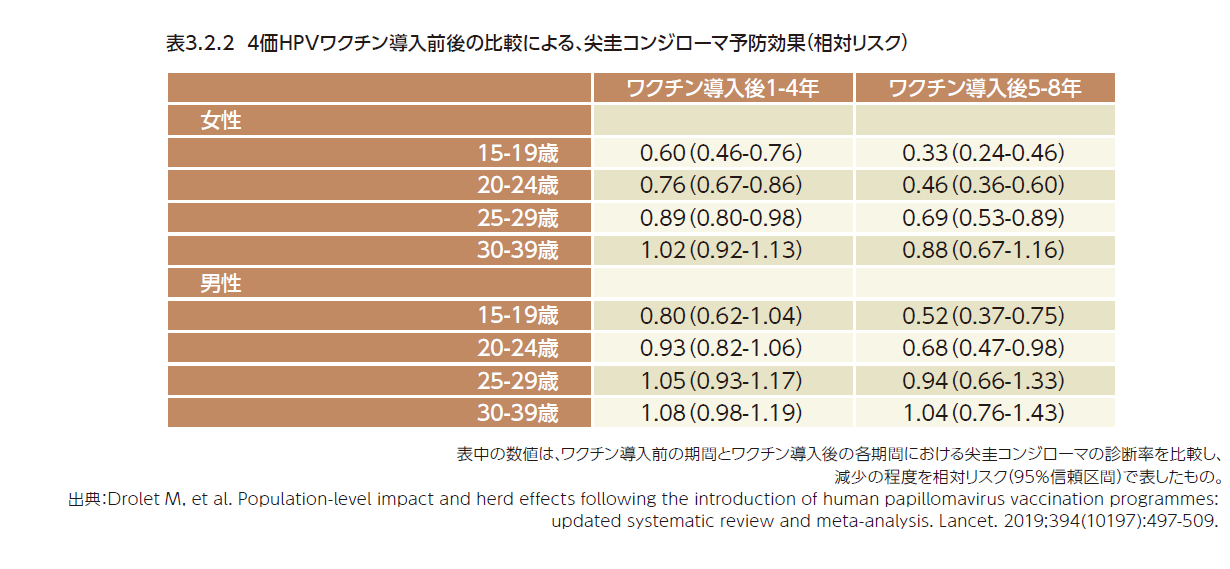
欧米諸国においてHPVワクチン導入前後の比較による効果を評価した研究のメタアナリシス8)では、4価HPVワクチン導入国における尖圭コンジローマ診断に対する予防効果もまとめられている。29論文(18研究)のメタアナリシスの結果、15歳~19歳の女性では、ワクチン導入前と比べて、ワクチン導入後5年~8年の時点で67%の減少が認められた。15歳~19歳の男性では、ワクチン導入前と比べて、ワクチン導入後5年~8年の時点で48%の減少が認められた。男性はワクチンを接種していないことから、女性の接種を介して集団免疫が成立したと考えられた1,8)(表3.2.2)。
③ 男性におけるHPV感染予防効果
男性におけるHPVワクチン接種による感染予防効果についても少ないが報告されている。2017年4月までの系統的レビューによると、肛門・性器におけるHPV16型、18型の持続感染に対する有効率はそれぞれ46.9%(95%信頼区間:28.6~60.8)、56.0%(95%信頼区間:28.8~73.7)、口腔においては88%(95%信頼区間:2~98)であった。研究開始時にHPV未感染(抗体陰性+PCR陰性)であった男性を対象とした場合、肛門・性器におけるHPV16、18型の持続感染に対する有効率は、それぞれ78.7%(95%信頼区間:55.5~90.9)、96.0%(95%信頼区間:75.6~99.9)とより高くなった14)。
引用文献
1)国立感染症研究所.9価ヒトパピローマウイルス(HPV)ワクチンファクトシート.2021年1月31日.
https://www.mhlw.go.jp/content/10906000/000770615.pdf,
(2023年2月21日アクセス)
2)Arbyn M, Xu L, Simoens C, et al. Prophylactic vaccination against human papillomaviruses to prevent cervical cancer and its precursors. Cochrane Database Syst Rev 2018;5(5): Cd009069.
3)Huh WK, Joura EA, Giuliano AR, et al. Final efficacy, immunogenicity, and safety analyses of a nine-valent human papillomavirus vaccine in women aged 16-26 years: a randomised, double-blind trial. Lancet 2017; 390(10108):2143-2159.
4)Garland SM, Pitisuttithum P, Ngan HYS, et al. Efficacy, Immunogenicity, and Safety of a 9-Valent Human Papillomavirus Vaccine: Subgroup Analysis of Participants From Asian Countries. J Infect Dis 2018; 218(1): 95-108.
5)Kudo R, Yamaguchi M, Sekine M, et al. Bivalent Human Papillomavirus Vaccine Effectiveness in a Japanese Population: High Vaccine-Type-Specific Effectiveness and Evidence of Cross-Protection. J Infect Dis 2019; 219(3): 382-390.
6)Wheeler CM, Castellsagué X, Garland SM, et al. Cross-protective efficacy of HPV-16/18 AS04-adjuvanted vaccine against cervical infection and precancer caused by non-vaccine oncogenic HPV types: 4-year end-of-study analysis of the randomised, double-blind PATRICIA trial. Lancet Oncol 2012; 13 (1): 100-110.
7)Tota JE, Struyf F, Sampson JN, et al. Efficacy of the AS04-Adjuvanted HPV16/18 Vaccine: Pooled Analysis of the Costa Rica Vaccine and PATRICIA Randomized Controlled Trials. J Natl Cancer Inst 2020; 112(8): 818-828.
8)Drolet M, Bénard É, Pérez N, Brisson M; HPV Vaccination Impact Study Group. Population-level impact and herd effects following the introduction of human papillomavirus vaccination programmes: updated systematic review and meta-analysis. Lancet. 2019;394(10197):497-509.
9)Karube A, Saito F, Nakamura E, et al. Reduction in HPV 16/18 prevalence among young women following HPV vaccine introduction in a highly vaccinated district, Japan, 2008-2017. J Rural Med 2019;14(1): 48-57.
10)米国National Cancer Institute. Human Papillomavirus (HPV) Vaccines.
https://www.cancer.gov/about-cancer/causes-prevention/risk/infectious-agents/hpv-vaccine-fact-sheet.
2021年5月25日,(2023年2月21日アクセス)
11)Petrosky E, Bocchini JA, Hariri S, et al. Use of 9-Valent Human Papillomavirus (HPV) Vaccine: Updated HPV Vaccination Recommendations of the Advisory Committee on Immunization Practices MMWR. 2015;64(11);300-304.
12)Lehtinen M, Apter D, Eriksson T, et al. Effectiveness of the AS04-adjuvanted HPV-16/18 vaccine in reducing oropharyngeal HPV infections in young females-Results from a community-randomized trial. Int J Cancer. 2020;147(1):170-174.
13)Nielsen KJ, Jakobsen KK, Jensen JS, et al. The Effect of Prophylactic HPV Vaccines on Oral and Oropharyngeal HPV Infection-A Systematic Review. Viruses. 2021;13(7):1339.
14)Harder T, Wichmann O, Klug SJ, et al. Efficacy, effectiveness and safety of vaccination against human papillomavirus in males: a systematic review. BMC Med. 2018;16(1):110.
3.2.2 HPVワクチンによるHPV関連がん予防効果
ワクチンの臨床的予防効果は、すでに述べた通り感染予防効果、発症予防効果、重症化予防効果に分けられる。HPVワクチンによるHPV関連がんの発症あるいは重症化予防効果を評価する場合のアウトカムは、前がん病変、がん罹患(浸潤がん)、がん死亡の各段階に分けて検討される。HPVワクチンが子宮頸部の前がん病変を予防する効果について科学的証拠は十分に蓄積されており、がん罹患(浸潤がん)予防の証拠も複数報告されている。
① 子宮頸部の前がん病変に対する予防効果
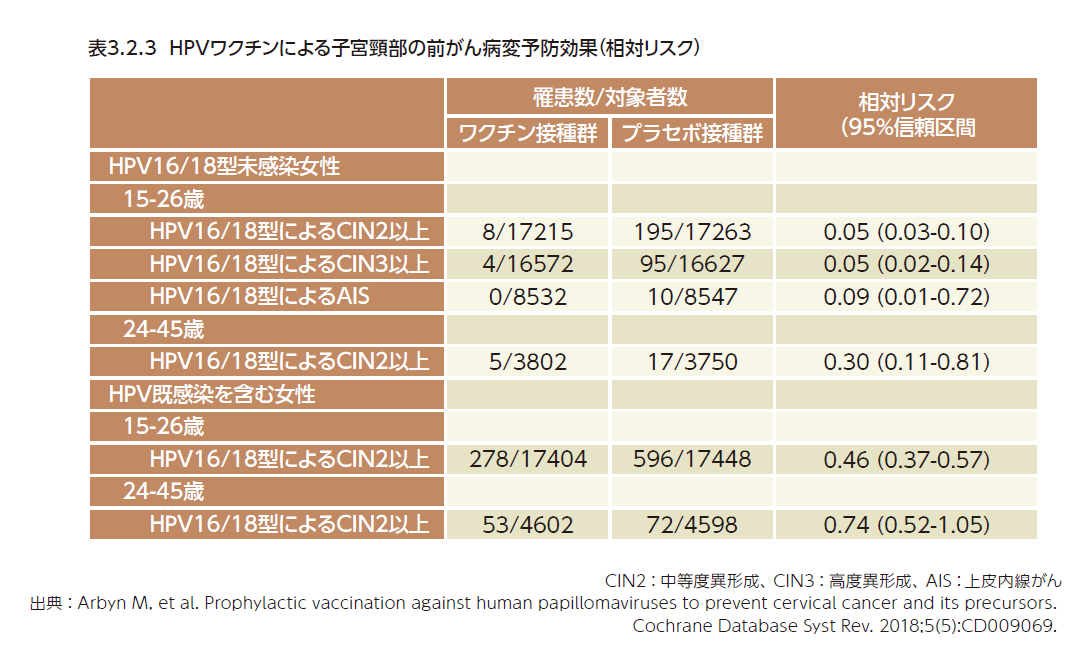
2価または4価HPVワクチンの第II相あるいは第Ⅲ相臨床試験(それぞれの追跡期間は最長で9年と6年)のメタアナリシスによると(計26試験、約74,000人)、HPV16、18型に未感染の15歳~26歳の女性(約17,000~34,000人、アウトカム指標により変動あり)では、HPV16、18型による子宮頸部の中等度異形成(CIN2)以上の病変、高度異形成(CIN3)以上の病変、上皮内腺がん(AIS)に対する相対リスクは、プラセボ投与群と比較してワクチン投与群で統計的に有意に低下し、それぞれ0.05(95%信頼区間:0.03~0.10)、0.05(95%信頼区間:0.02~0.14)、0.09(95%信頼区間:0.01~0.72)であった。ワクチン有効率に換算すると、95%、95%、91%であり、いずれも非常に高い予防効果が認められた。24歳~45歳の女性(約7,600人)に限った場合も、CIN2以上の病変に対する中程度の予防効果(有効率70%)が認められた。ワクチン接種時点で既にHPVに感染している女性も含めると、15歳~26歳の女性ではCIN2以上の病変に対する予防効果が中程度に低下し(有効率54%)、24歳~45歳の女性では有意な予防効果が認められなかった(表3.2.3)1,2)。
英国では、2008年の2価HPVワクチンの導入から10年以上が経過している。2価ワクチンの有効性を調査するため、大規模ながん登録データを使用し、ワクチン接種群(計3群:12歳~13歳で接種を受けた群、14歳~16歳でキャッチアップ接種を受けた群、16歳~18歳でキャッチアップ接種を受けた群)と非接種群(ワクチン導入前の群)について、2006年1月~2019年6月の期間におけるCIN3病変の発生率の比較を行った。計1,370万人年の追跡期間中、CIN3病変に対するワクチン有効率は、非接種群と比較して、16歳~18歳接種群で39%(95%信頼区間:36~41)、14歳~16歳接種群で75%(72~77)、12歳~13歳接種群で97%(96~98)であった。また、ワクチン接種により17,235例のCIN3病変を予防できたと推定された3)。
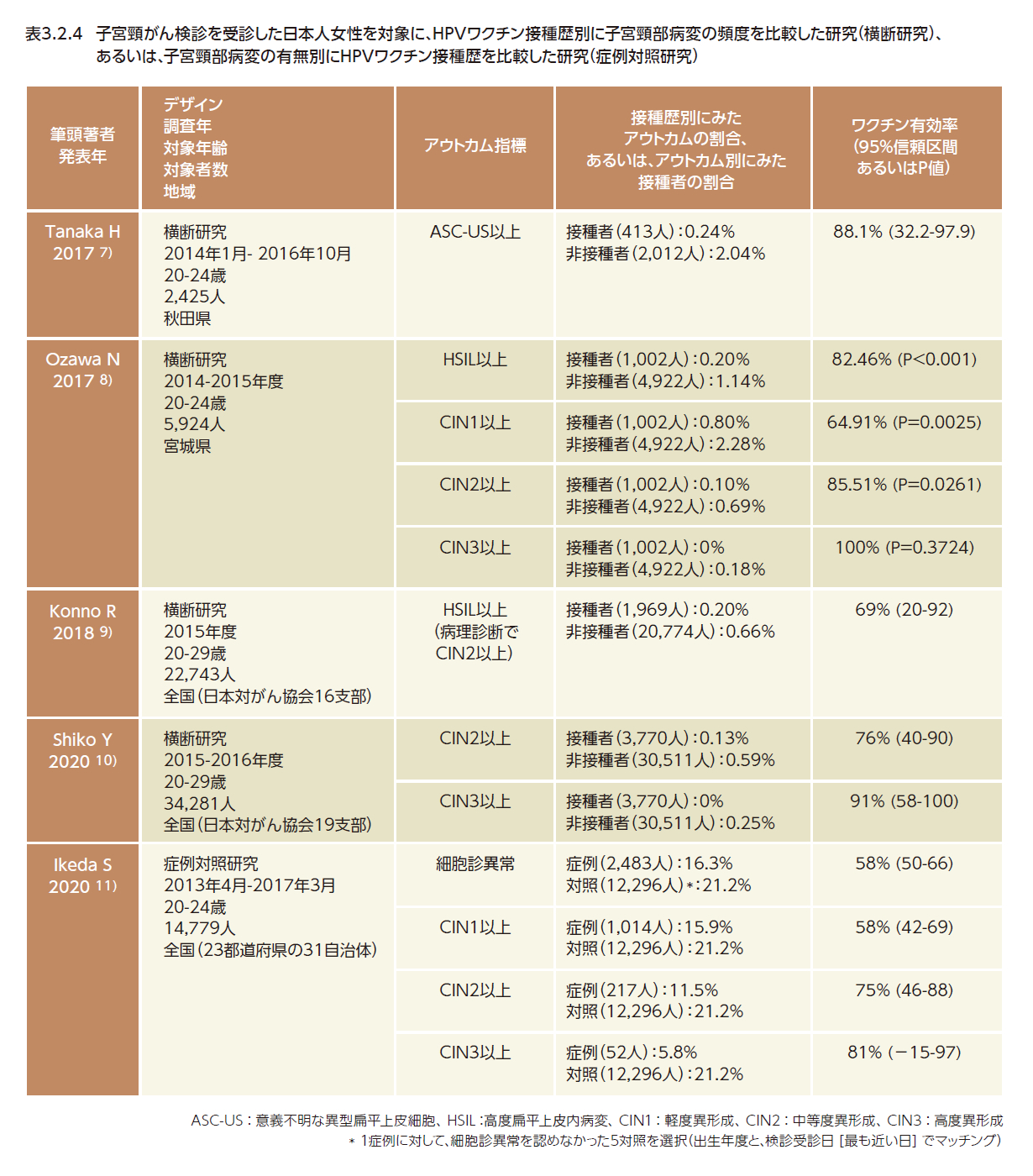
日本からも、臨床試験や疫学研究の結果が多数報告されている。2価HPVワクチンの第II相臨床試験で、2価HPVワクチンに含まれる遺伝子型に未感染の20歳~25歳女性を長期間追跡した結果によると、最初の接種から4年の時点で、HPV16、18型による子宮頸部の軽度異形成(CIN1)以上の病変の発生は、ワクチン投与群(406人)で0人、比較(A型肝炎ワクチン投与)群(404人)で8人であり、予防効果は100%(95%信頼区間:42.2~100)であった1,4)。4価HPVワクチンの第Ⅱ相臨床試験では、4価ワクチンに含まれる遺伝子型に未感染の18歳~26歳女性を対象にワクチン投与群(509人)とプラセボ投与群(アジュバントのみ含有、512人)で比較した結果、最初の接種から2.5年の時点で、HPV6、11、16、18型によるCIN1あるいはCIN2病変はすべてプラセボ投与群でのみ認められた1,5)。4価HPVワクチンの単群オープンラベル臨床試験では、4価HPVワクチンに含まれる遺伝子型に未感染の女性(16歳~26歳、967人)に最初に接種してから4年の時点で、HPV6、11、16、18型によるCIN1以上の病変は認められなかった1,6)。また、子宮頸がん検診の受診者を対象に、HPVワクチン接種歴別に子宮頸部病変の頻度を比較した横断研究、あるいは、子宮頸部病変の有無別にHPVワクチン接種歴を比較した症例対照研究では、おおむね60%~90%の予防効果を認めている1,7–11)(表3.2.4)。
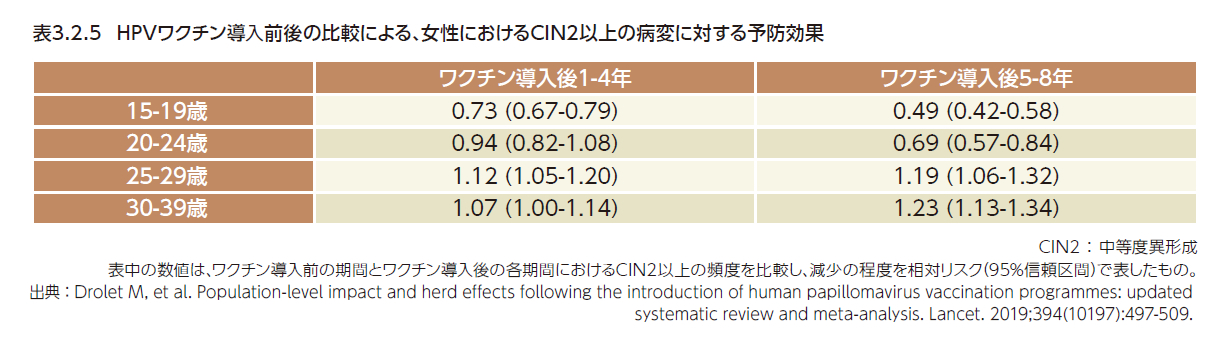
HPVワクチン接種を国家プログラムに含めている欧米諸国で、ワクチン導入前後の比較による前がん病変予防効果が評価されるとともに、これらの報告の大規模なメタアナリシスも行われている。2014年2月1日から2018年10月11日の期間に公表された13論文(9研究)のメタアナリシスの結果、15歳~19歳の女性では、ワクチン導入前と比べて、ワクチン導入後5年~8年の時点で、CIN2以上の病変に対して51%の減少が示された。20歳~24歳の女性では31%の減少にとどまることから、性交渉開始前の女性にHPVワクチンを接種することが重要であることが示された1,12)(表3.2.5)。
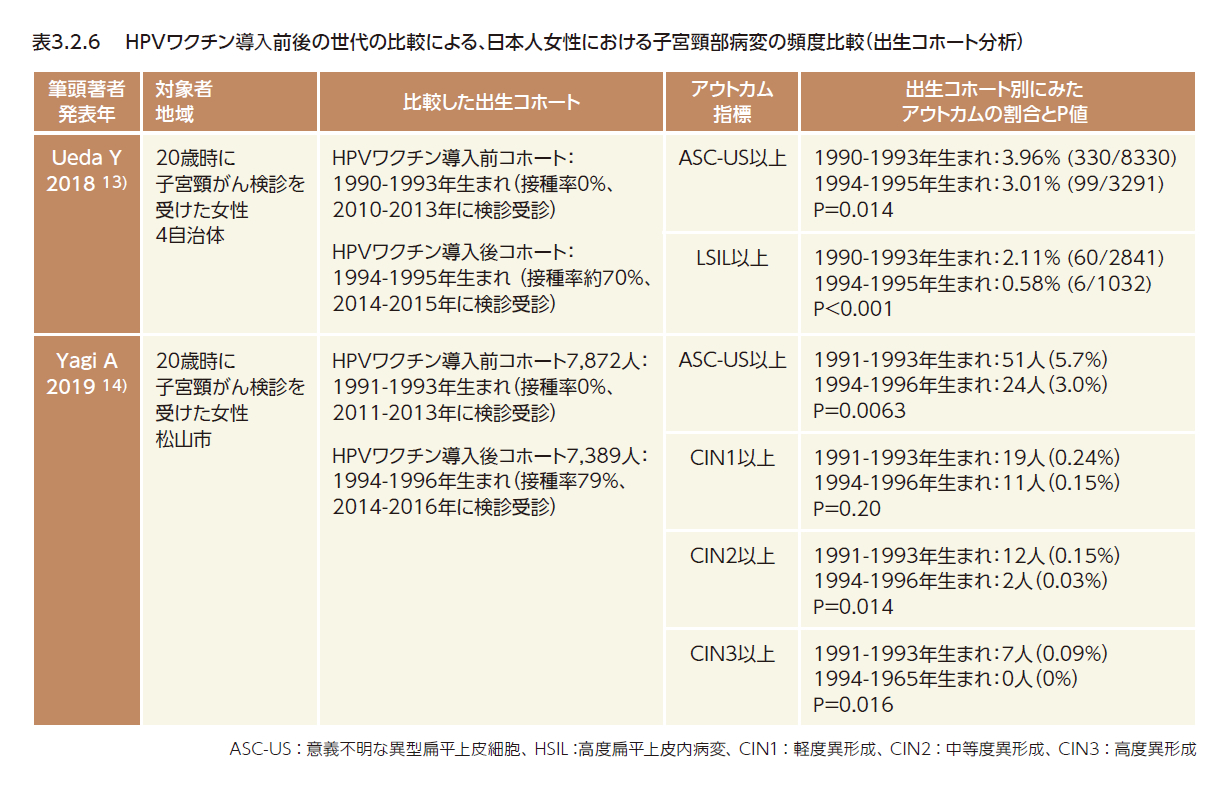
日本でも、ワクチン導入前後の世代の比較(出生コホート分析)により、前がん病変の予防効果が認められている。表3.2.6に示すいずれの研究も、ワクチン導入前の世代(1990年~1993年生まれ、あるいは、1991年~1993年生まれ)と比較して、ワクチン導入後の世代(1994年~1995年生まれ、あるいは、1994年~1996年生まれ)では、前がん病変の頻度が有意に低下していた1,13,14)。
2価あるいは4価のHPVワクチン接種から少なくとも10年~12年後までは、ワクチンに含まれる遺伝子型のHPV感染による子宮頸部前がん病変の発生を予防する効果が持続すると考えられる1)。臨床試験の長期追跡の中間解析によると、9歳~15歳で9価HPVワクチンを3回接種した女性971人では、約8年後の時点で、9種類のHPV型が原因の高度子宮頸部疾患は1例も認められなかった1,15)。
交差免疫の持続期間については、2価HPVワクチン接種後4年の時点で、HPV31、33型によるCIN2以上の病変(HPV16、18型の共感染を除く)に対する予防効果(59%~84%)が報告されている。しかし、追跡期間が長くなると一部の型の持続感染に対する予防効果が低下するとの報告もあることから、交差免疫の持続期間についてはさらに長期の成績が必要である1)。
② 子宮頸がん罹患に対する予防効果
日本を含めた18か国105施設で、16歳~26歳の健康女性(14,215人)を対象に行われた9価HPVワクチンのランダム化二重盲検試験では、浸潤性の子宮頸がんを含む高度子宮頸部疾患に対する予防効果が検証されている。比較対照は4価HPVワクチンで、9価HPVワクチンで追加された5つのHPV型(HPV31, 33, 45, 52, 58)に関連した疾患の罹患率が評価された。初回接種前から3回目接種後1か月までHPV非感染であった者では、ワクチン初回接種から最長6年(中央値4年)の時点での高度子宮頸部疾患(CIN2/3、AIS、浸潤性子宮頸がん)の発生率は、9価HPVワクチン接種群で10,000人年あたり0.5人、4価HPVワクチン接種群で18.1人であり、有効率は97.1%(95%信頼区間:83.5~99.9)であった1,16)。
2価および4価HPVワクチンの国際共同第Ⅲ相臨床試験のうち、フィンランドでの長期追跡結果が公表され、HPV関連浸潤がんに対する有効性が初めて報告された。14歳~19歳の女性において、ワクチン非接種群(17,838人)で10人のHPV関連浸潤がん患者(うち8人が子宮頸がん)が発生したのに対し、ワクチン接種群(9,529人)では0人で、予防効果は100%(95%信頼区間:16~100)であった1,17)。
スウェーデンでは、全国データベースを用いて、10歳~30歳の女性を対象に4価HPVワクチンの浸潤性子宮頸がんに対する予防効果が評価された。2006年1月1日以降、10歳以上の女性を2017年12月31日あるいは31歳の誕生日を迎えるまで追跡した。分析対象となった1,672,983人のうち子宮頸がんと診断された者は、接種者527,871人中19人、非接種者1,145,112人中538人であった。診断時の年齢を調整した相対リスクは0.51(95%信頼区間:0.32~0.82)であり、さらに暦年、居住地方、親の学歴・収入、母親の出身国・がん罹患歴を調整した相対リスクは0.37(0.21~0.57)であった。ワクチン接種時の年齢別にみた相対リスクは、17歳未満で接種した場合は0.12(0.00~0.34)、17歳~30歳で接種した場合は0.47(0.27~0.75)であり、性交渉開始前の女子にHPVワクチンを接種することが、子宮頸がんの予防に重要であることが改めて示唆された1,18)。
デンマークでは、HPVワクチン接種と子宮頸がん診断の全国登録の情報を使用して、2006年10月から2019年12月に17歳~30歳であった地域在住女性867,689人を対象に、HPVワクチン接種による子宮頸がん予防効果が評価された。接種時に子宮頸がんが潜在していた影響を考慮するため、バッファー期間を1年ごとに設定した(例:バッファー期間が1年間の場合、実際に接種を受けた後も1年間は非接種と扱う)。計5,544,655人年の追跡期間中、504人が子宮頸がんと診断され、325人が非接種者、179人が接種者(ほとんどが20歳~30歳で接種)であった。1年間のバッファー期間を設定した多変量解析では、16歳以下、17歳~19歳、20歳~30歳でワクチンを接種した女性の子宮頸がんに対する相対リスクは、ワクチン非接種の女
性と比較して、それぞれ0.14(95%信頼区間:0.04~0.53)、0.32(0.08~1.28)、1.19(0.80~1.79)であった。バッファー期間を長くしても、16歳以下、17歳~19歳でワクチンを接種した女性の結果はほとんど変わらなかったが、20歳~30歳でワクチンを接種した女性では相対リスクが徐々に減少し、バッファー期間を4年間とした場合の相対リスクは0.85(0.55-1.32)と1を下回った。この結果は、20歳~30歳では接種を受けた時点で子宮頸がんが潜在していることを示唆するものであり、HPVワクチン接種を低年齢で行うことが重要であることを示している19)。
前がん病変に対する2価HPVワクチンの予防効果を示した英国の研究(既出)では3)、子宮頸がん予防効果も検証しており、ワクチン有効率は、16歳~18歳接種群で34%(95%信頼区間:25~41)、14歳~16歳接種群で62%(95%信頼区間:52~71)、12歳~13歳接種群で87%(95%信頼区間:72~94)であった。また、ワクチン接種により448例の子宮頸がんを予防できたと推定された。
日本では、2013年4月~2017年3月に31自治体(23都道府県)で子宮頸がん検診を受診した20歳~24歳の女性を対象に症例対照研究が実施され、細胞診異常を認めた2,483例の症例と、細胞診異常を認めなかった12,296例の対照について、過去のワクチン接種歴が比較されている1,11)(表3.2.4)。症例のうち8人が子宮頸がんと診断されており、すべてワクチン非接種者であった。
③ 子宮頸部以外の部位に発生するHPV関連がん疾患の前がん病変に対する予防効果
日本を含めた18か国105施設で、16歳~26歳の健康女性(14,215人)を対象に行われた9価HPVワクチンのランダム化二重盲検試験(既出、比較対照は4価HPVワクチン)では、子宮頸部以外の部位に発生するHPV関連がん疾患の前がん病変に対する予防効果も検証されている。初回接種前から3回目接種後1か月までHPV非感染であった者での外陰部や膣の軽度異形成(VIN1あるいはVAIN1)の罹患は、4価ワクチン接種群では6,012人中13人、9価ワクチン接種群では6,009人中1人であった(有効率:92.3%、95%信頼区間:54.6-99.6)。高度外陰部疾患(VIN2/3、外陰がん)は両群ともに罹患者がなく評価できなかった。高度膣疾患(VAIN2/3、膣がん)の罹患は、4価ワクチン接種群では6,012人中3人、9価ワクチン接種群では6,009人中0人であった(有効率:100%、95%信頼区間:-71.5~100)1,16)。
④ 接種スケジュール、キャッチアップ接種
HPVワクチンは当初3回接種のスケジュールで承認されたが、WHOの提言1,20)により2014年から2回接種スケジュールが各国で承認され、実施されている(3.5参照)。この変更は、9歳~14歳の女性に2回接種したときの幾何平均抗体価が、上の年代の女性(15歳~26歳)に3回接種して得られる幾何平均抗体価と同等かそれ以上というデータに基づいている1)。なお、免疫抑制状態にある者には、少なくとも2回接種し、可能であれば3回目も接種することが推奨されている1,21)。1回接種による効果についても近年エビデンスが蓄積されつつあり22–26)、WHOは2022年12月に、1回接種は2回接種あるいは3回接種と同等のHPV感染予防効果があると提言した21)。これらの証拠はHPV感染をアウトカムとした研究であり、前がん病変に対する予防効果については、今後の研究結果が待たれる。
HPVワクチン接種の機会を逃した女性を対象に実施されているキャッチアップ接種(3.1参照)では、標準とされている接種間隔より長い間隔で2回目あるいは3回目接種が行われる場合がある。HPVワクチンの接種スケジュールについては、8年以上の接種間隔が空いた場合のエビデンスは国内外で認められていないが、現状入手可能なエビデンスによれば、1年~5年の接種間隔が空いた場合の海外の研究においては、通常の接種スケジュールと比較して一定程度の免疫原性と安全性が示されている27)。また、キャッチアップ接種では、標準的な接種年齢(ワクチン接種による利益がリスクを最も上回ると期待される年齢)よりも、高い年齢で接種を受けることになる。米国予防接種諮問委員会の勧告では、27歳以上でのキャッチアップ接種は推奨しておらず、接種する場合は個別の医学的判断によるとされている28)。メタアナリシスや海外の研究によると、HPV未感染女性においては高年齢での接種であっても有効性は認められているが、低年齢で接種した場合に比べて有効性は低く、既にHPVに感染している場合には十分な効果が得られないことが示されている1–3,12,18,19)。日本でも、全国21医療機関でCIN2-3/AISと診断された40歳未満の女性を対象に、HPVワクチンを最初に接種した年齢層別にHPV16、18型陽性率を比較したところ、13歳~16歳で12.5%、17歳~20歳で14.3%、21歳~25歳で35.3%、26歳以上で39.4%であり、20歳未満と20歳以上の比較で有意差が認められた1,29)。キャッチアップ接種の対象者には、可能な限り20歳までの早い時期に接種を受けるよう推奨するとともに、20歳以降の子宮頸がん検診をより積極的に推奨する必要がある。
⑤ 男性におけるHPVワクチン接種による前がん病変予防効果
男性にHPVワクチンを接種した場合の前がん病変予防効果についても少ないが報告されている。2017年4月までの系統的レビューによると、肛門の上皮内腫瘍に対する有効率は、中等度異形成の場合は61.9%(95%信頼区間:21.4~82.8)(ランダム化二重盲検試験)あるいは50%(95%信頼区間:2~74)(コホート研究)、高度異形成の場合は46.8%(95%信頼区間:-20~77.9)であった。研究開始時にHPV未感染(抗体陰性+PCR陰性)であった男性を対象とした場合の有効率は、中等度異形成に対して75.8%(95%信頼区間:-16.9~97.5)、高度異形成に対して63.7%(95%信頼区間:-103~96.4)であった30)。
引用文献
1)国立感染症研究所.9価ヒトパピローマウイルス(HPV)ワクチンファクトシート.2021年1月31日.
https://www.mhlw.go.jp/content/10900000/001014059.pdf
2)Arbyn M, Xu L, Simoens C, et al. Prophylactic vaccination against human papillomaviruses to prevent cervical cancer and its precursors. Cochrane Database Syst Rev. 2018;5(5):CD009069.
3)Falcaro M, Castañon A, Ndlela B, et al. The effects of the national HPV vaccination programme in England, UK, on cervical cancer and grade 3 cervical intraepithelial neoplasia incidence: a register-based observational study. Lancet. 2021;398(10316):2084-2092.
4)Konno R, Yoshikawa H, Okutani M, et al. Efficacy of the human papillomavirus (HPV)-16/18 AS04-adjuvanted vaccine against cervical intraepithelial neoplasia and cervical infection in young Japanese women. Hum Vaccin Immunother. 2014;10(7):1781-1794..
5)Yoshikawa H, Ebihara K, Tanaka Y, et al. Efficacy of quadrivalent human papillomavirus (types 6, 11, 16 and 18) vaccine (GARDASIL) in Japanese women aged 18-26 years. Cancer Sci. 2013;104(4):465-472.
6)Sakamoto M, Miyagi E, Sumi Y, et al. Effectiveness on high-grade cervical abnormalities and long-term safety of the quadrivalent human papillomavirus vaccine in Japanese women. J Infect Chemother. 2019;25 (7):520-525.
7)Tanaka H, Shirasawa H, Shimizu D, et al. Preventive effect of human papillomavirus vaccination on the development of uterine cervical lesions in young Japanese women. J Obstet Gynaecol Res. 2017;43 (10):1597-1601.
8)Ozawa N, Ito K, Tase T, et al. Lower Incidence of Cervical Intraepithelial Neoplasia among Young Women with Human Papillomavirus Vaccination in Miyagi, Japan. Tohoku J Exp Med. 2017;243(4):329-334.
9)Konno R, Konishi H, Sauvaget C, et al. Effectiveness of HPV vaccination against high grade cervical lesions in Japan. Vaccine. 2018;36 (52):7913-7915.
10)Shiko Y, Konno R, Konishi H, et al. Effectiveness of HPV vaccination against the development of high-grade cervical lesions in young Japanese women. BMC Infect Dis. 2020;20(1):808. Published 2020 Nov 5.
11)Ikeda S, Ueda Y, Hara M, et al. Human papillomavirus vaccine to prevent cervical intraepithelial neoplasia in Japan: A nationwide case-control study. Cancer Sci. 2021;112(2):839-846.
12)Drolet M, Bénard É, Pérez N, et al. Population-level impact and herd effects following the introduction of human papillomavirus vaccination programmes: updated systematic review and meta-analysis. Lancet. 2019;394(10197):497-509.
13)Ueda Y, Yagi A, Nakayama T, et al. Dynamic changes in Japan’s prevalence of abnormal findings in cervical cervical cytology depending on birth year [published correction appears in Sci Rep. 2018 Sep 3;8 (1):13384]. Sci Rep. 2018;8(1):5612.
14)Yagi A, Ueda Y, Ikeda S, et al. Evaluation of future cervical cancer risk in Japan, based on birth year. Vaccine. 2019;37(22):2889-2891.
15)Olsson SE, Restrepo JA, Reina JC, et al. Long-term immunogenicity, effectiveness, and safety of nine-valent human papillomavirus vaccine in girls and boys 9 to 15 years of age: Interim analysis after 8 years of follow-up. Papillomavirus Res. 2020;10:100203.
16)Huh WK, Joura EA, Giuliano AR, et al. Final efficacy, immunogenicity, and safety analyses of a nine-valent human papillomavirus vaccine in women aged 16-26 years: a randomised, double-blind trial. Lancet. 2017;390(10108):2143-2159.
17)Luostarinen T, Apter D, Dillner J, et al. Vaccination protects against invasive HPV-associated cancers. Int J Cancer. 2018;142(10):2186-2187.
18)Lei J, Ploner A, Elfström KM, et al. HPV Vaccination and the Risk of Invasive Cervical Cancer. N Engl J Med. 2020;383(14):1340-1348.
19)Kjaer SK, Dehlendorff C, Belmonte F, et al. Real-World Effectiveness of Human Papillomavirus Vaccination Against Cervical Cancer. J Natl Cancer Inst. 2021;113(10):1329-1335.
20)World Health Organization. Weekly epidemiological record. No. 21, 2014, 89, 221‒236.
https://cdn.who.int/media/docs/default-source/immunization/sage/2014/april/apr2014wer8921.pdf?sfvrsn=83c7d7b1_3,
(2023年2月23日アクセス)
21)World Health Organization. Human papillomavirus vaccines: WHO position paper, December 2022. Weekly Epidemiological Record No 50, 2022, 97, 645–672 .
https://www.who.int/publications/i/item/who-wer9750-645-672,
(2023年2月23日アクセス)
22)Kreimer AR, Sampson JN, Porras C, et al. Evaluation of Durability of a Single Dose of the Bivalent HPV Vaccine: The CVT Trial. J Natl Cancer Inst. 2020;112(10):1038-1046.
23)Sankaranarayanan R, Joshi S, Muwonge R, et al. Can a single dose of human papillomavirus (HPV) vaccine prevent cervical cancer? Early findings from an Indian study. Vaccine. 2018;36(32 Pt A):4783-4791
24)Basu P, Malvi SG, Joshi S, et al. Vaccine efficacy against persistent human papillomavirus (HPV) 16/18 infection at 10 years after one, two, and three doses of quadrivalent HPV vaccine in girls in India: a multicentre, prospective, cohort study [published correction appears in Lancet Oncol. 2022 Jan;23(1):e16]. Lancet Oncol. 2021;22(11):1518-1529.
25)Whitworth HS, Gallagher KE, Howard N, et al. Efficacy and immunogenicity of a single dose of human papillomavirus vaccine compared to no vaccination or standard three and two-dose vaccination regimens: A systematic review of evidence from clinical trials. Vaccine. 2020;38(6):1302-1314.
26)Barnabas RV, Brown ER, Onono MA, et al. Efficacy of single-dose HPV vaccination among young African women. NEJM Evid. 2022;1 (5):EVIDoa2100056.
27)厚生労働省.第47回厚生科学審議会予防接種・ワクチン分科会予防接種基本方針部会(資料1)HPVワクチンについて. 2022年1月27日.
https://www.mhlw.go.jp/content/10601000/000890273.pdf,
(2023年2月6日アクセス)
28)Meites E, Szilagyi PG, Chesson HW, et al. Human Papillomavirus Vaccination for Adults: Updated Recommendations of the Advisory Committee on Immunization Practices. Morbidity and Mortality Weekly Report (MMWR) 2019;68(32);698–702.
29)Matsumoto K, Yaegashi N, Iwata T, et al. Reduction in HPV16/18 prevalence among young women with high-grade cervical lesions following the Japanese HPV vaccination program. Cancer Sci. 2019;110 (12):3811-3820.
30)Harder T, Wichmann O, Klug SJ, van der Sande MAB, Wiese-Posselt M. Efficacy, effectiveness and safety of vaccination against human papillomavirus in males: a systematic review. BMC Med. 2018;16(1):110.
3.2.3 HPVワクチンの安全性
ワクチンの安全性の考え方では、有害事象(adverse event)と有害反応(adverse reaction;副反応ともいう)を区別する。有害事象とは、ワクチン接種後に生じたあらゆる好ましくない事象であり、ワクチン接種との因果関係を問わない。有害反応(副反応)は、有害事象のうち、ワクチン接種との因果関係が否定できない事象である。有害反応(副反応)は、通常、局所反応と全身反応に分けられる。
① 接種後の局所反応と全身反応
HPVワクチン接種後の局所反応は、高頻度に発現する。9価HPVワクチンの臨床試験では、接種者の72%~95%に何らかの局所反応が認められた。報告頻度の高かった症状は、接種部位の痛み(55%~93%)、腫れ(9%~49%)、紅斑(9%~42%)で、これらの症状のために就労や日常生活に支障があるなどの重症例は、痛みが0%~6%、腫れ(5cm以上)が1%~10%、紅斑(5cm以上)が0%~3%であった1)。米国における承認後ワクチンの有害事象報告制度(Vaccine Adverse Event Reporting System: VAERS)のデータによると、2014年12月から2017年12月の期間に報告された9価HPVワクチン接種後の有害事象7,244件のうち(対象期間の9価ワクチンの出荷本数は27,996,934本)、接種部位の痛みが316件(4.5%)、紅斑が314件(4.4%)であった1,2)。
HPVワクチン接種後の全身反応の頻度は、局所反応よりも低いものの、一定程度発現する。9価HPVワクチンの臨床試験では、接種者の35%~60%に何らかの全身反応が認められ、ワクチン接種に関連すると判断された者の割合は14%~31%であった。報告頻度の高かった症状は、頭痛(2%~20%)、発熱(2%~9%)、嘔気(1%~4%)、めまい(1%~3%)、疲労感(0%~3%)であった。重篤と判断された者(致命的・継続的で重篤な後遺症あり、入院例、先天異常、がん、など)は0%~3%であり、ワクチン接種に関連すると判断された者は0%~0.3%であった1)。米国VAERS(既出)のデータによると、2014年12月から2017年12月の期間に報告された9価HPVワクチン接種後の有害事象7,244件のうち、報告が多かった全身反応は、めまい(8.0%)、失神(6.7%)、頭痛(5.8%)であった1,2)。
接種後反応の1つとして、稀ではあるが失神も報告されている。9価ワクチンの第III相臨床試験のうち7試験のデータを統合した分析では、9価ワクチン接種後の失神の発現頻度は0.2%であり、1回目接種後の発現が最も多い。ほとんどは女性で、失神が起こった後に受けた接種で再び失神した者はいなかった1,3)。米国疾病予防管理センター(Centers for Disease Control and Prevention:CDC)と健康保険システムが共同で運営する、ワクチンの安全性を評価する制度(Vaccine Safety Datalink:VSD)において、9価ワクチンを接種した18歳~26歳女性で失神を起こす頻度は、ほかのワクチンを接種した同年代の女性よりも高かった1,4)。失神後の転倒による外傷などを避けるため、接種後しばらくは座位や臥位で安静を保ち、経過観察を行うことが推奨されている5)。国内で承認されている製剤の添付文書でも、2価、4価、9価ワクチンいずれについても、接種後30分程度は座らせるなどした上で状態を観察することが望ましいとされている。
9価ワクチンの臨床試験で、4価ワクチンを比較対照とした結果によると、9価ワクチン接種者では、4価ワクチン接種者と比較して、局所反応、全身反応ともに発現頻度が高く、全身反応では1.07倍~1.24倍であった1)。また、9価ワクチンの第Ⅲ相臨床試験のうち7試験のデータを統合した分析(既出)1,3)で、安全性の性差を評価したところ、9価ワクチン接種後に報告された局所反応や全身反応の内容は女性と男性で同様であったが、各症状の報告頻度は女性の方が男性より高かった。
② 接種後の有害事象
9価ワクチンの第Ⅲ相臨床試験のうち7試験のデータを統合分析した研究によると(既出、2試験は4価ワクチンが比較対照)1,3)、自己免疫疾患を示唆する症状が発現した頻度は、9価ワクチン接種者(3.9%;7,092人中274人)と4価ワクチン接種者(3.6%;7,093人中252人)で同程度であった。症状の内容も同様であり、頻度が高かったのは関節痛(9価:1.8%、4価:1.7%)と甲状腺の異常(9価:1.2%、4価:1.0%)であった。その他の症状は報告頻度が低く(0.1%以下)、多様で複数の身体的部位にまたがる症状であった。1つの試験では、4価ワクチン接種者と9価ワクチン接種者のうち、それぞれ1人ずつが複合性局所疼痛症候群(Complex Regional Pain Syndrome:CRPS)と診断され、いずれも以前の怪我が原因と判断された。9価ワクチン接種者のうち、2人が体位性頻脈症候群(Postural orthostatic tachycardia syndrome:POTS)と診断された。このうち1人は再接種時に症状の再発を認めず、もう1人はワクチン接種後3年以上経過後の発症であったため、時間的関連に乏しいと判断された。
自己免疫疾患については6研究のメタアナリシス1,6)、フランスで行われた症例対照研究7,8)、およびフィンランドで全国規模のデータベースを用いて行われた後ろ向きコホート研究7,9)、POTSについては米国VAERSの情報を用いた検討7,10)、長期疲労についてはオランダのプライマリケアデータベースを用いた後ろ向きコホート研究7,11)などが行われているが、いずれも、HPVワクチン接種との関連なし、あるいは、安全性のシグナルは検出されなかったと結論づけられている。
韓国では、HPVワクチン接種後の重篤な有害事象を評価するため、2017年1月から2019年12月までに国のデータベース(ワクチン接種者および健康情報データベース)に登録された情報に基づき、一次分析としてコホート研究、二次分析として自己対照リスク期間デザイン(self-controlled risk interval design)による評価が行われた。自己対照リスク期間デザインとは、1人の個人の時間経過の中で、ワクチン接種後の有害事象が生じやすいと考えられる期間(リスク期間)と、生じにくいと考えらえる期間(対照期間)を設定し、それぞれの期間における有害事象の発現頻度を比較する方法である。2017年に、HPVワクチン、日本脳炎ワクチン、成人用三種混合(百日せきジフテリア破傷風混合)ワクチンのいずれかを接種した11歳から14歳の女性441,399人のうち、382,020人がHPVワクチンを接種した。重篤な有害事象は、内分泌疾患、消化器疾患、循環器疾患、神経疾患などに分類し、全33の事象について評価した。一次分析では片頭痛のみ、HPVワクチン接種群でリスクの増加を認めた(罹患率比=1.11,95%信頼区間:1.02~1.22)。二次分析ではいずれの事象も、HPVワクチン接種後のリスク期間における頻度の増加は認められなかった7,12,13)。
2価および4価HPVワクチンの有効性と安全性を評価したランダム化比較試験の系統的レビューでは26件の研究が検討され、HPVワクチン接種群と対照群(ほかのワクチンを接種またはアジュバントのみ接種)における重篤な有害事象の報告は同程度であった(相対リスク=0.98,95%信頼区間:0.92~1.05)。HPVワクチン接種群における死亡者数は、対照群における死亡者数の1.29倍(95%信頼区間:0.85~1.98)であったが、信頼区間からみて、ワクチン接種と死亡の関連性は低いと判断された1,14)。
9価HPVワクチンの臨床試験で接種後の死亡が0%~0.1%の頻度で報告されているが、各試験で設置されている効果安全性評価委員会によって、いずれもワクチン接種とは関連がないと判断されている。また、何らかの接種後有害事象が発生したために所定の回数の接種を完了できなかった者が、0%~0.3%の頻度で報告されている1)。
③ 接種後の「疼痛または運動障害を中心とする多様な症状」
国内では、2013年4月1日にHPVワクチンが定期接種A類に位置づけられた後、接種後に「疼痛または運動障害を中心とする多様な症状」が発現することが報告された(3.4.1参照)。2013年6月14日に開催された厚生科学審議会予防接種・ワクチン分科会副反応検討部会および薬事・食品衛生審議会医薬品等安全対策部会安全対策調査会(合同開催、以下、審議会)では、これらの症状の発生頻度などがより明らかになり、国民に対して適切な情報提供ができるようになるまでの間、定期接種を積極的に勧奨すべきではないとされ、同日、健康局長通知が発出された(3.3参照)。当該症状は、2014年1月20日開催の審議会で「針を刺した痛みや薬液による局所の腫れなどをきっかけとして心身の反応が惹起され、症状が慢性化した可能性が高い」と一定の合意を得たものの(2014年7月4日開催の審議会で「機能性身体症状と同義」と整理)、結論を得るには至らなかった。厚生労働省が実施した副反応追跡調査によると、当該症状の発現頻度は0.005%であり(接種者約338万人中、未回復186人)、極めて稀であることが示された15)。
審議会の委員意見を受けて設置された厚生労働科学研究費補助金「子宮頸がんワクチンの有効性と安全性の評価に関する疫学研究」(研究代表者:祖父江友孝)では、2016年に、全国の病院から層化無作為抽出した11,037診療科を対象として、多様な症状による受診状況に関する全国疫学調査を実施した。症状の持続期間や就学・就労への影響なども考慮した、12歳~18歳における多様な症状の有訴率(調査対象期間:2015年7月~12月)は、男性、HPVワクチン接種歴のない女性ともに、人口10万人あたり20人と推計された。すなわち、HPVワクチン接種歴のない青少年においても多様な症状を有する者が一定数存在した1,16,17)。
別途、名古屋市で実施された地域ベースの疫学調査では、2015年8月時点で名古屋市に在住し、2010年4月時点で9歳~15歳の女性29,846人を対象に、HPVワクチン接種歴の有無別に24項目の多様な症状を比較した。症状の出現頻度は、HPVワクチン接種者と未接種者で同様であった1,18)。
その後、審議会で国内外の最新の知見を引き続き整理した結果、改めてHPVワクチンの安全性について特段の懸念が認められないことが確認され、接種による有効性が副反応のリスクを明らかに上回ると認められた。2021年11月12日開催の審議会で積極的勧奨の再開が決定され、同年11月26日に健康局長通知が発出された。2022年4月1日以降は、接種の機会を逃した方々へのキャッチアップ接種も含め、個別勧奨が行われている(3.3参照)。積極的な勧奨の再開後、接種者数が増加しているが、ワクチンの安全性に特段の懸念は示されていない19)。
④ 予防接種ストレス関連反応
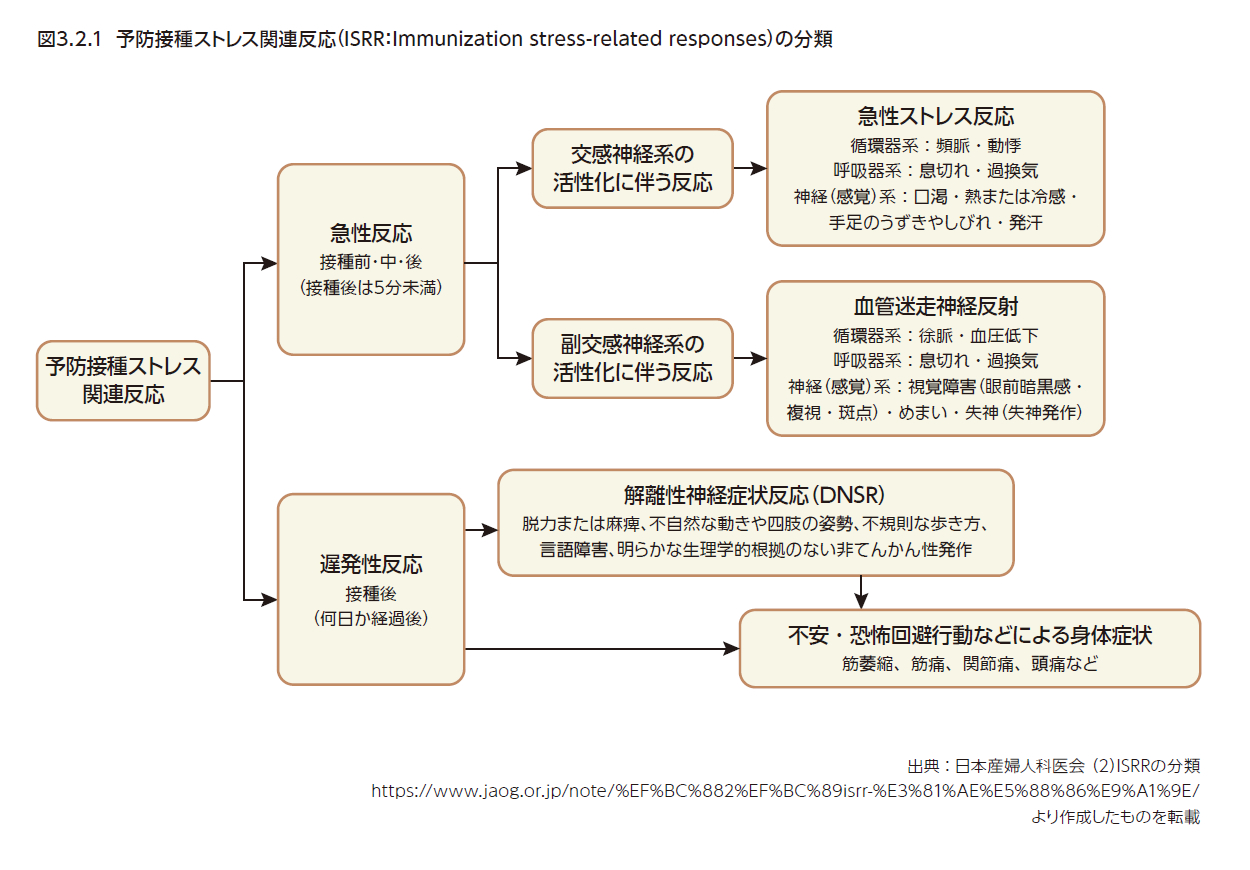
2019年、世界保健機関(WHO)は、ワクチン接種後に認められる「機能性身体症状」に関連して、予防接種ストレス関連反応(以下、ISRR:Immunization stress-related responses)という概念を提唱し、医療従事者などが見過ごさないよう呼びかけた20)。ISRRの特徴は、ワクチンの種類には関係なく、ワクチン接種への不安や、注射針への恐怖や痛みなどにより、接種の前後に過呼吸やめまい、痛み、不随意運動、しびれ、手足の動かしにくさなどを起こすものとしている。ISRRには、接種前や接種中、接種後5分未満に起こる「急性反応」と、接種後数日してから起こる「遅発性反応」がある(図3.2.1)。「急性反応」には交感神経系の活性化による動悸、過換気、息切れ、発汗などの急性ストレス反応と、副交感神経系の活性化による血圧低下や徐脈、めまい、失神などの血管迷走神経反射がある。「遅発性反応」には脱力、麻痺、異常な動きや四肢の姿勢、言語障害、非てんかん発作などの「解離性神経症状反応(Dissociative Neurological Symptom Reaction:DNSR)」があげられ、さらに、長期間続く痛みや不安などは、身体を動かさないことによる二次性の廃用症候群や抑うつ、治療依存などの問題を生じさせ、単純な生物学的メカニズムで説明のつかない多様な症状を作りだすことがある(なお、これらは必ずしもDNSRの後に生じるわけではない)。ISRRは、あらゆる年代で接種されるすべてのワクチンによって生じうる。予防のためには、接種者による丁寧な説明、丁寧な接種、信頼関係の構築が必要である20–23)。
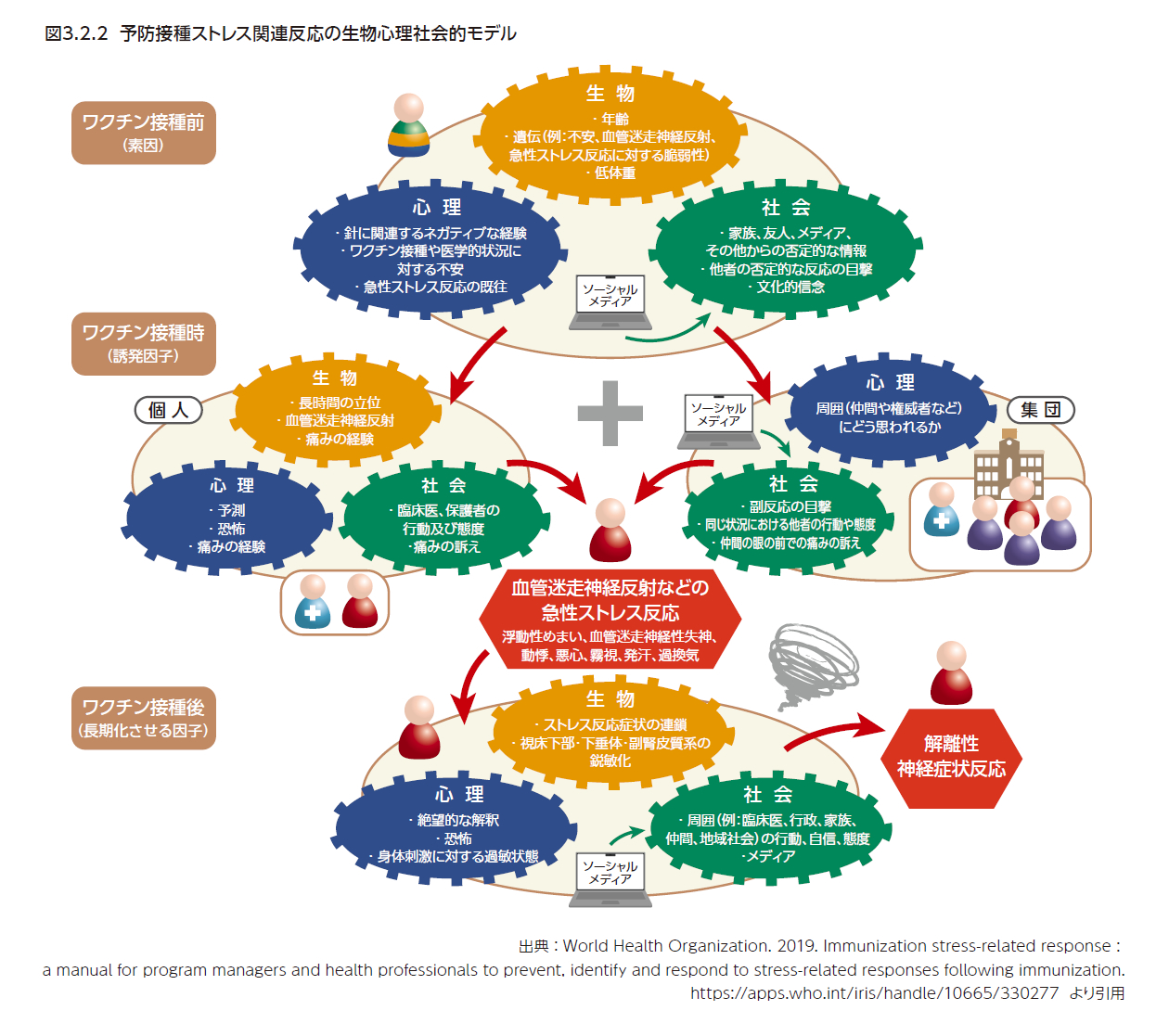
DNSRでは、知覚や運動が障害されているが、様々な検査を行っても器質的には原因は特定できない。このDNSRの中で接種後約7日以内に発症したものが接種ストレスに関連していると考えられているが、ISRRはその個人の年齢やBody Mass Indexといった「生物学的要素」、針への恐怖やワクチンに対する不安といった「精神心理学的要素」、友達やメディアからのネガティブな情報や目撃といった「社会的要素」が複雑にからみあって成り立つという生物心理社会モデルが提唱されている20)(図3.2.2)。これら3つの要素は、接種前(素因)、接種時(誘発因子)、接種後(長期化させる因子)、それぞれの段階で作用する。ワクチンの接種にあたっては、事前に医療従事者がこれらについて十分に理解し、必要に応じて接種時の不安を軽減させるような環境調整やコミュニケーションがワクチン接種後の「機能性身体症状」の発生予防、診断、コントロールに重要と考えられる。また、これらの症状が出現した際に医療機関が連携して対応し、いわゆる「たらい回し」が起こらないよう留意すると同時に、不適切な医療などを行わないようなことが求められる(3.4参照)。
引用文献
1)国立感染症研究所.9価ヒトパピローマウイルス(HPV)ワクチンファクトシート.2021年1月31日.
https://www.mhlw.go.jp/content/10900000/001014059.pdf,
(2022年11月22日アクセス)
2)Shimabukuro TT, Su JR, Marquez PL, Mba-Jonas A, Arana JE, Cano MV. Safety of the 9-Valent Human Papillomavirus Vaccine. Pediatrics. 2019;144(6):e20191791.
3)Moreira ED Jr, Block SL, Ferris D, et al. Safety Profile of the 9-Valent HPV Vaccine: A Combined Analysis of 7 Phase III Clinical Trials. Pediatrics. 2016;138(2):e20154387.
4)Donahue JG, Kieke BA, Lewis EM, et al. Near Real-Time Surveillance to Assess the Safety of the 9-Valent Human Papillomavirus Vaccine. Pediatrics. 2019;144(6):e20191808. doi:10.1542/peds.2019-1808
5)米国National Cancer Institute.「Human Papillomavirus (HPV) Vaccines」. 2021年5月25日.
https://www.cancer.gov/about-cancer/causes-prevention/risk/infectious-agents/hpv-vaccine-fact-sheet,
(2022年11月22日アクセス)
6)Genovese C, LA Fauci V, Squeri A, Trimarchi G, Squeri R. HPV vaccine and autoimmune diseases: systematic review and meta-analysis of the literature. J Prev Med Hyg. 2018;59(3):E194-E199. Published 2018 Sep 28.
7)厚生労働省.第69回厚生科学審議会予防接種・ワクチン分科会副反応検討部会.令和3年度第18回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(2021年10月1日合同開催)資料1-2:HPVワクチンの安全性・有効性に関する最新のエビデンスについて
https://www.mhlw.go.jp/stf/shingi2/0000208910_00031.html,
(2022年11月22日アクセス)
8)Grimaldi-Bensouda L, Rossignol M, Koné-Paut I, et al. Risk of autoimmune diseases and human papilloma virus (HPV) vaccines: Six years of case-referent surveillance. J Autoimmun. 2017;79:84-90. doi:10.1016/j.jaut.2017.01.005
9)Skufca J, Ollgren J, Artama M, Ruokokoski E, Nohynek H, Palmu AA. The association of adverse events with bivalent human papilloma virus vaccination: A nationwide register-based cohort study in Finland. Vaccine. 2018;36(39):5926-5933.
10)Arana J, Mba-Jonas A, Jankosky C, et al. Reports of Postural Orthostatic Tachycardia Syndrome After Human Papillomavirus Vaccination in the Vaccine Adverse Event Reporting System. J Adolesc Health. 2017;61 (5):577-582.
11)Schurink-Van’t Klooster TM, Kemmeren JM, van der Maas NAT, et al. No evidence found for an increased risk of long-term fatigue following human papillomavirus vaccination of adolescent girls. Vaccine. 2018;36(45):6796-6802.
12)厚生労働省.「令和4年4月からのHPVワクチンの接種について」2022年3月11日.
https://www.mhlw.go.jp/content/10906000/000911549.pdf,
(2022年11月22日アクセス)
13)Yoon D, Lee JH, Lee H, Shin JY. Association between human papillomavirus vaccination and serious adverse events in South Korean adolescent girls: nationwide cohort study. BMJ. 2021;372:m4931. Published 2021 Jan 29.
14)Arbyn M, Xu L. Efficacy and safety of prophylactic HPV vaccines. A Cochrane review of randomized trials. Expert Rev Vaccines. 2018;17 (12):1085-1091.
15)厚生労働省.第15回厚生科学審議会予防接種・ワクチン分科会副反応検討部会,平成27年度第4回薬事・食品衛生審議会医薬品等安全対策部会安全対策調査会(2015年9月17日合同開催)資料4-1「副反応追跡調査結果について」.
https://www.mhlw.go.jp/file/05-Shingikai-10601000-Daijinkanboukouseikagakuka-Kouseikagakuka/0000097681.pdf,
(2022年11月22日アクセス)
16)祖父江友孝.第23回厚生科学審議会予防接種・ワクチン分科会副反応検討部会,平成28年度第9回薬事・食品衛生審議会医薬品等安全対策部会安全対策調査会(2016年12月26日合同開催)資料4「全国疫学調査(子宮頸がんワクチンの有効性と安全性の評価に関する疫学研究)」.
https://www.mhlw.go.jp/file/05-Shingikai-10601000-Daijinkanboukouseikagakuka-Kouseikagakuka/0000147016.pdf,
(2022年11月22日アクセス)
17)Fukushima W, Hara M, Kitamura Y, et al. A Nationwide Epidemiological Survey of Adolescent Patients With Diverse Symptoms Similar to Those Following Human Papillomavirus Vaccination: Background Prevalence and Incidence for Considering Vaccine Safety in Japan. J Epidemiol. 2022;32(1):34-43.
18)Suzuki S, Hosono A. No association between HPV vaccine and reported post-vaccination symptoms in Japanese young women: Results of the Nagoya study. Papillomavirus Res. 2018;5:96-103.
19)厚生労働省.「薬事・食品衛生審議会(HPVワクチン副反応被害判定調査会)」.
https://www.mhlw.go.jp/stf/shingi/shingi-yakuji_366199.html,
(2023年3月2日アクセス)
20)World Health Organization.「Immunization stress-related response: a manual for program managers and health professionals to prevent, identify and respond to stress-related responses following immunization」. 2019年12月20日.
https://www.who.int/publications/i/item/9789241515948
(日本語版:
https://www.mhlw.go.jp/content/10601000/000962339.pdf),
(2022年11月15日アクセス)
21)日本産科婦人科学会.「子宮頸がんとHPVワクチンに関する正しい理解のために」.
https://www.jsog.or.jp/modules/jsogpolicy/index.php?content_id=4,
(2022年11月15日アクセス)
22)日本産婦人科医会.思春期の予防接種と接種ストレス関連反応.
https://www.jaog.or.jp/note/%e6%80%9d%e6%98%a5%e6%9c%9f%e3%81%ae%e4%ba%88%e9%98%b2%e6%8e%a5%e7%a8%ae%e3%81%a8%e6%8e%a5%e7%a8%ae%e3%82%b9%e3%83%88%e3%83%ac%e3%82%b9%e9%96%a2%e9%80%a3%e5%8f%8d%e5%bf%9c/,
(2022年11月15日アクセス)
23)日本小児科学会.「知っておきたいわくちん情報:予防接種ストレス関連反応(ISRR)」.
https://www.jpeds.or.jp/modules/activity/index.php?content_id=263,
(2022年11月15日アクセス)
3.3 日本におけるHPVワクチン接種の経緯・現状
① HPVワクチン接種の経緯
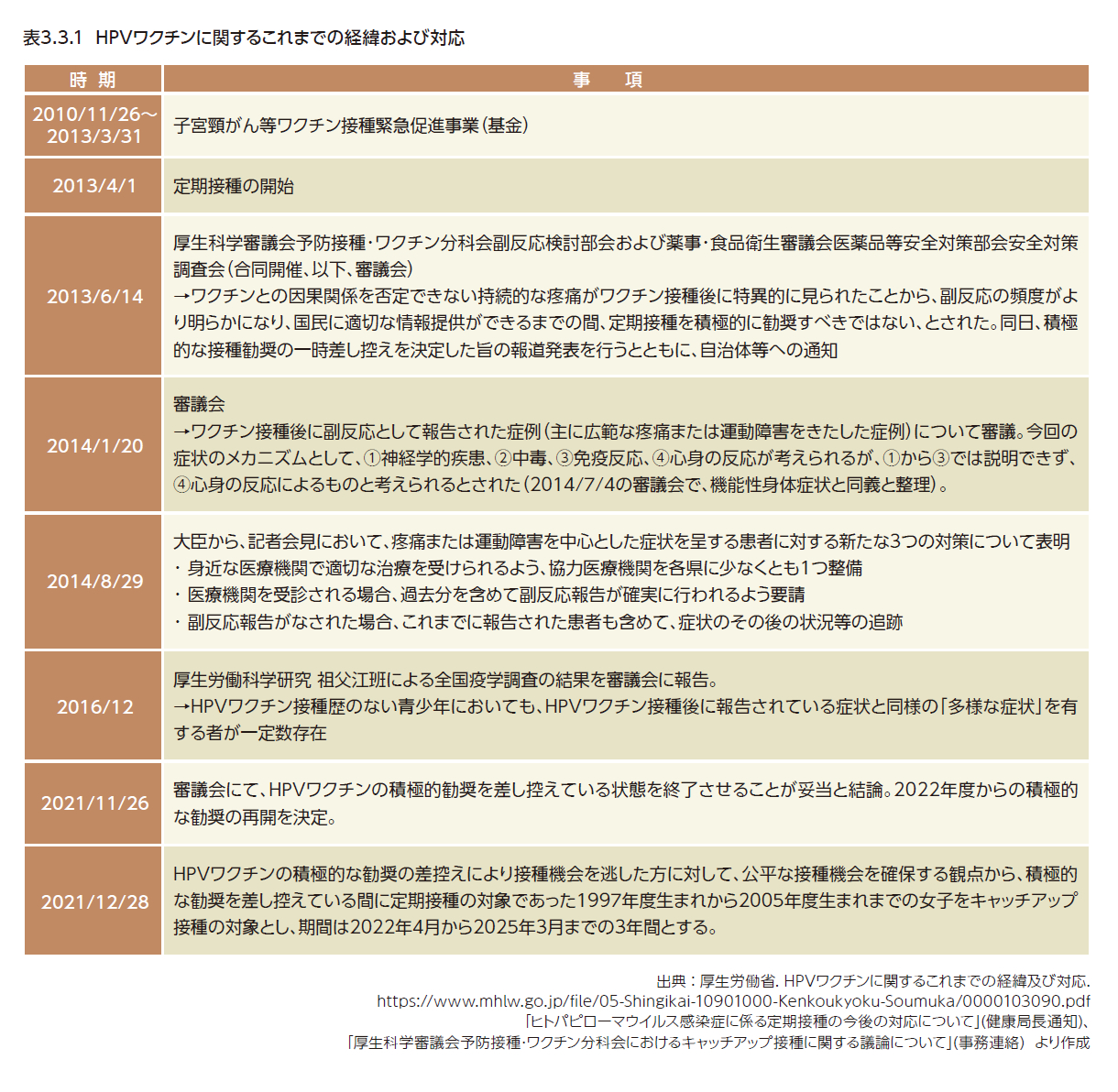
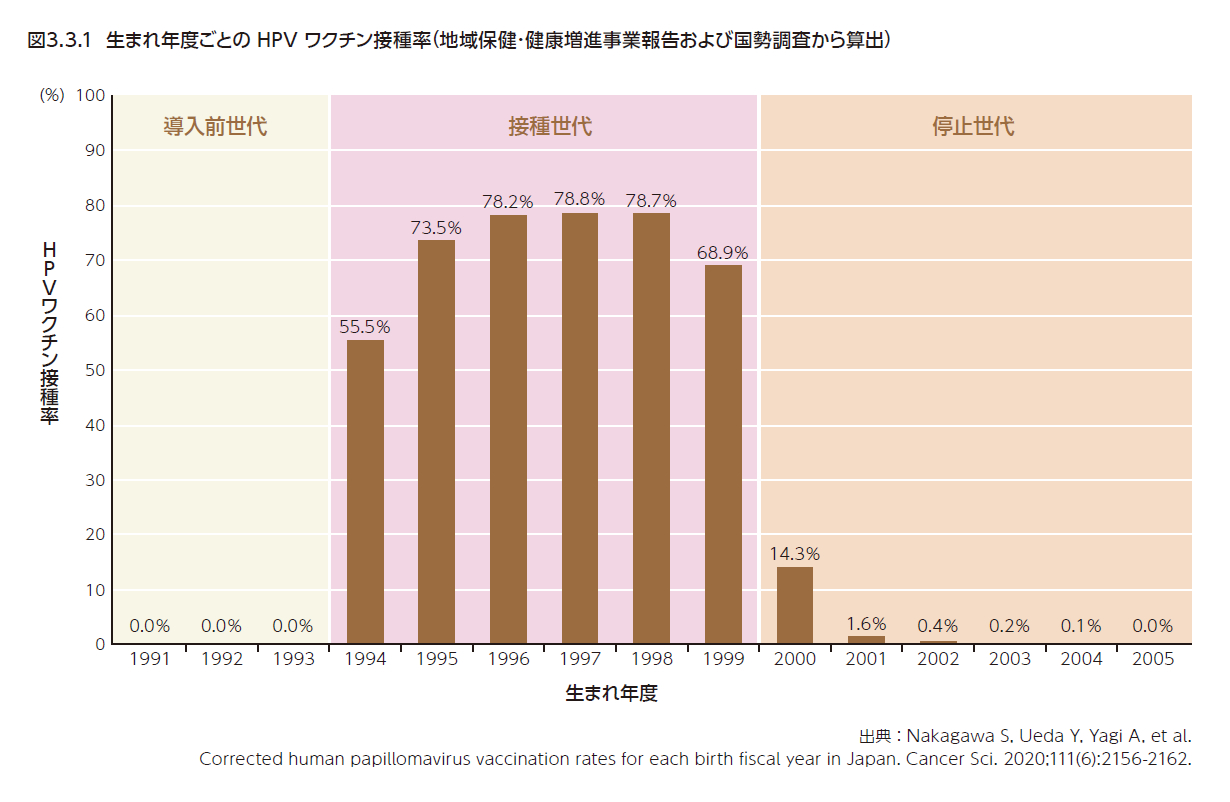
わが国では、子宮頸がんおよびその前がん病変の罹患率を減少させ、子宮頸がんの死亡率を減少させることを目的に、2010年11月26日から、子宮頸がん等ワクチン接種緊急促進事業が開始され、2013年4月1日より、小学校6年生~高校1年生相当の女性を対象とした国の予防接種プログラムにHPVワクチンが定期接種として導入された1)(表3.3.1)。しかし、広範な疼痛または運動障害を中心とした多様な症状が報告され、マスコミなどで多く報道された。2013年6月14日に開催された厚生科学審議会予防接種・ワクチン分科会副反応検討部会および薬事・食品衛生審議会医薬品等安全対策部会安全対策調査会(合同開催、以下、審議会)にて、ワクチンとの因果関係を否定できない持続的な疼痛の頻度がより明らかになり、国民に適切な情報提供ができるようになるまでの間、定期接種を積極的に推奨すべきではない、とされ、同日、積極的な接種勧奨の一時差し控えが勧告された2,3)。こうした経緯から、HPVワクチン接種率は、1997年度生まれの約80%をピークに急落し、2002年度以降に生まれた女性の接種率は1%未満まで低下した4)(図3.3.1)。また、ワクチン非接種世代において、ワクチン接種世代よりも細胞診異常率の増加が報告された5)。2014年1月20日および7月4日に開催された審議会では、HPVワクチン接種後に生じた「多様な症状」の病態とその因果関係について評価され、接種後に慢性的な疼痛などの身体症状は認められるが、「多様な症状」については、医学的検査で症状に見合う異常が認められない病態である「機能性身体症状」と定義された(3.2.3参照)。また、2016年12月、厚生労働科学研究費補助金「子宮頸がんワクチンの有効性と安全性の評価に関する疫学研究」(研究代表者:祖父江友孝)による全国疫学調査にて、HPVワクチン接種歴のない青少年においても、HPVワクチン接種後に報告されている症状と同様の「多様な症状」を有する者が一定数存在することが報告された6)。その後、審議会において、HPVワクチンの有効性および安全性に関する評価、HPVワクチン接種後に生じた症状への対応、HPVワクチンについての情報提供の取組みなどについて継続的に議論が行われ、2021年11月12日に開催された審議会において、最新の知見を踏まえ、改めてHPVワクチンの安全性について特段の懸念が認められないことが確認され、接種による有効性が副反応のリスクを明らかに上回ると認められた7)。また、HPVワクチンの積極的勧奨を差し控えている状態については、引き続きHPVワクチンの安全性の評価を行っていくこと、接種後に生じた症状の診療に係る協力医療機関の診療実態の継続的な把握や体制強化を行っていくこと、都道府県や地域の医療機関などの関係機関の連携を強化し地域の支援体制を充実させていくこと、HPVワクチンについての情報提供を充実させていくこと、などの今後の対応の方向性も踏まえつつ、2021年11月26日にHPVワクチン定期接種の積極的勧奨差し控えが終了とされた8)。これを受けて、2022年4月より、自治体における定期接種の個別勧奨が再開された。また、積極的勧奨差し控えにより接種機会を逃した者に対して公平な接種機会を確保する観点から、従来の定期接種の対象年齢を超えて接種を行う「キャッチアップ接種」が、2022年度~2024年度の3年間実施されることになった9)。
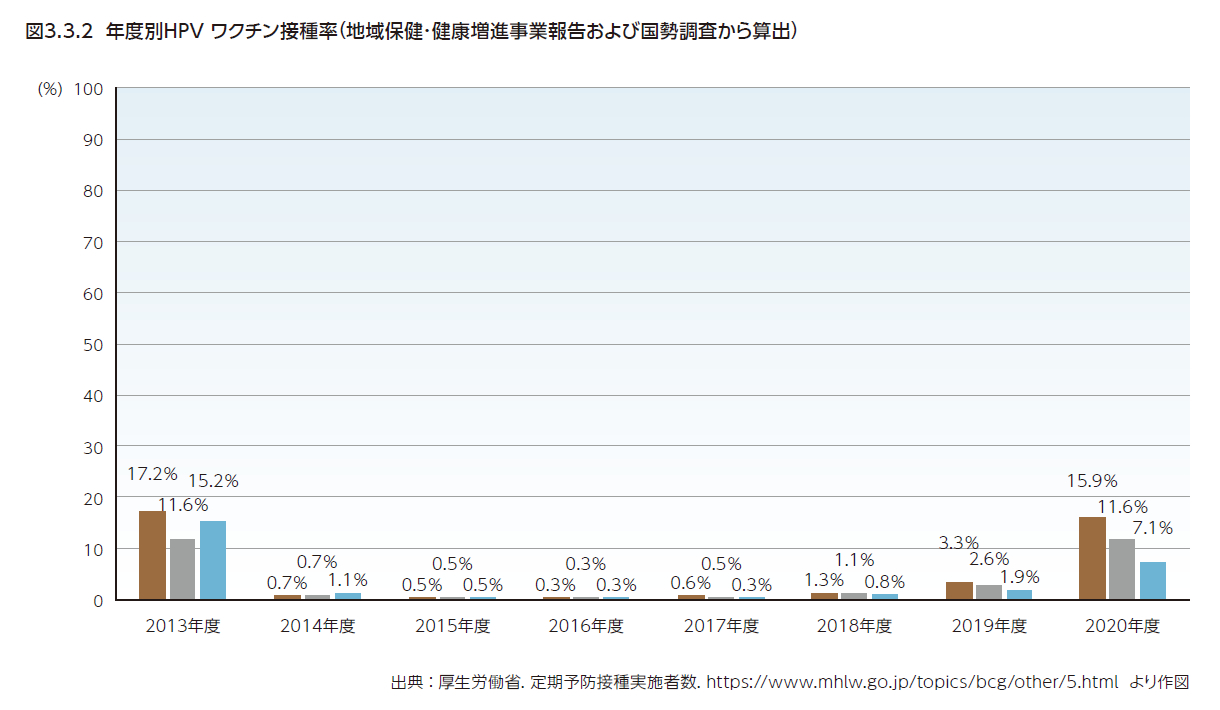
② HPVワクチン接種率と接種率向上の障壁
HPVワクチンの効果が期待される中、積極的勧奨の差し控えがあり、わが国におけるHPVワクチン接種率が非常に低い状態が継続した(図3.3.2)。2020年度のHPVワクチン接種率は、地域保健・健康増進事業報告「定期の予防接種被接種者数」より、1回目15.9%、2回目11.6%、3回目7.1%程度と推定される10)。2022年4月から9月までの実施状況についてはそれぞれ30.1%、18.8%、7.5%と推定され10)、回復の兆候が見られるが11)、HPVワクチンの普及が進んでいる諸外国と比べて著しく低い。また、2022年度のキャッチアップ接種対象の女性の調査によると、「接種したい」と回答した女性の割合は13.6%~25.7%程度にとどまっていた11)。
HPVワクチンの接種率が低い理由として、定期接種対象年齢の娘への接種をためらう母親の心理、つまり、将来子宮頸がんになるリスクより、今起こるかもしれない副反応のリスクを重んじて考えてしまう現在志向バイアスや、周囲の友人がHPVワクチンの接種をしていない状況をみて、自分だけ接種に向かえない、いわば負の同調効果などがあると指摘されている12)。わが国において子宮頸がんの発症を減少させるためには、少なくとも約50%の接種率がキャッチアップ接種で必要だというシミュレーション結果が示されている13)。接種率が80%近くであった1990年代後半生まれの世代と同等まで子宮頸がんのリスクを低減するには、2022年度内に90%程度のキャッチアップ接種率が必要との試算もある11)。積極的勧奨の差し控えにより大幅に下がった接種率を回復し、実効性のある子宮頸がん予防につなげるためには、早急にHPVワクチン接種を普及させることが強く求められている。
引用文献
1)Ikeda S, Ueda Y, Yagi A, et al. HPV vaccination in Japan: what is happening in Japan?. Expert Rev Vaccines. 2019;18(4):323-325 .
2)厚生労働省.ヒトパピローマウイルス感染症の定期接種の対応について(勧告).2013年6月14日
https://www.mhlw.go.jp/bunya/kenkou/kekkaku-kansenshou28/pdf/kankoku_h25_6_01.pdf,
(2023年2月6日アクセス)
3)厚生労働省.「2013年6月14日 第2回厚生科学審議会予防接種・ワクチン分科会副反応検討部会議事録」.
https://www.mhlw.go.jp/stf/shingi2/0000091965.html,
(2023年2月6日アクセス)
4)Nakagawa S, Ueda Y, Yagi A, et al. Corrected human papillomavirus vaccination rates for each birth fiscal year in Japan. Cancer Sci. 2020;111 (6):2156-216.
5)Yagi A, Ueda Y, Ikeda S, et al. The looming health hazard: A wave of HPV-related cancers in Japan is becoming a reality due to the continued suspension of the governmental recommendation of HPV vaccine. Lancet Reg Health West Pac. 2021;18:100327.
6)祖父江友孝.厚生労働科学研究費補助金「子宮頸がんワクチンの有効性と安全性の評価に関する疫学研究」2017年度分担研究報告書.
https://mhlw-grants.niph.go.jp/project/26725,
(2023年2月6日アクセス)
7)厚生労働省.「令和3年11月12日 第72回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和3年度第22回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(合同開催)議事録」.
https://www.mhlw.go.jp/stf/newpage_22253.html,
(2023年2月6日アクセス)
8)厚生労働省.ヒトパピローマウイルス感染症に係る定期接種の今後の対応について.
https://www.mhlw.go.jp/content/000875155.pdf,
(2023年2月6日アクセス)
9)厚生労働省.厚生科学審議会予防接種・ワクチン分科会におけるキャッチアップ接種に関する議論について(事務連絡).2021年12月28日.
https://www.mhlw.go.jp/content/000875153.pdf,
(2023年2月6日アクセス)
10)厚生労働省.第90回厚生科学審議会予防接種・ワクチン分科会副反応検討部会、令和4年度第23回薬事・食品衛生審議会薬事分科会医薬品等安全対策部会安全対策調査会(資料3-1)HPVワクチンの実施状況について.2023年1月20日.
https://www.mhlw.go.jp/content/10601000/001039949.pdf,
(2023年2月19日アクセス)
11)Yagi A, Ueda Y, Nakagawa S, et al. Can Catch-Up Vaccinations Fill the Void Left by Suspension of the Governmental Recommendation of HPV Vaccine in Japan?. Vaccines (Basel). 2022;10(9):1455.
12)Yagi A, Ueda Y, Kimura T. A behavioral economics approach to the failed HPV vaccination program in Japan. Vaccine. 2017;35(50):6931-6933.
13)Simms KT, Hanley SJB, Smith MA, et al. Impact of HPV vaccine hesitancy on cervical cancer in Japan: a modelling study. Lancet Public Health. 2020;5(4):e223-e234.
3.4 HPVワクチン接種後の症状とその対応
3.4.1 HPVワクチン接種後に生じた症状:日本の事例
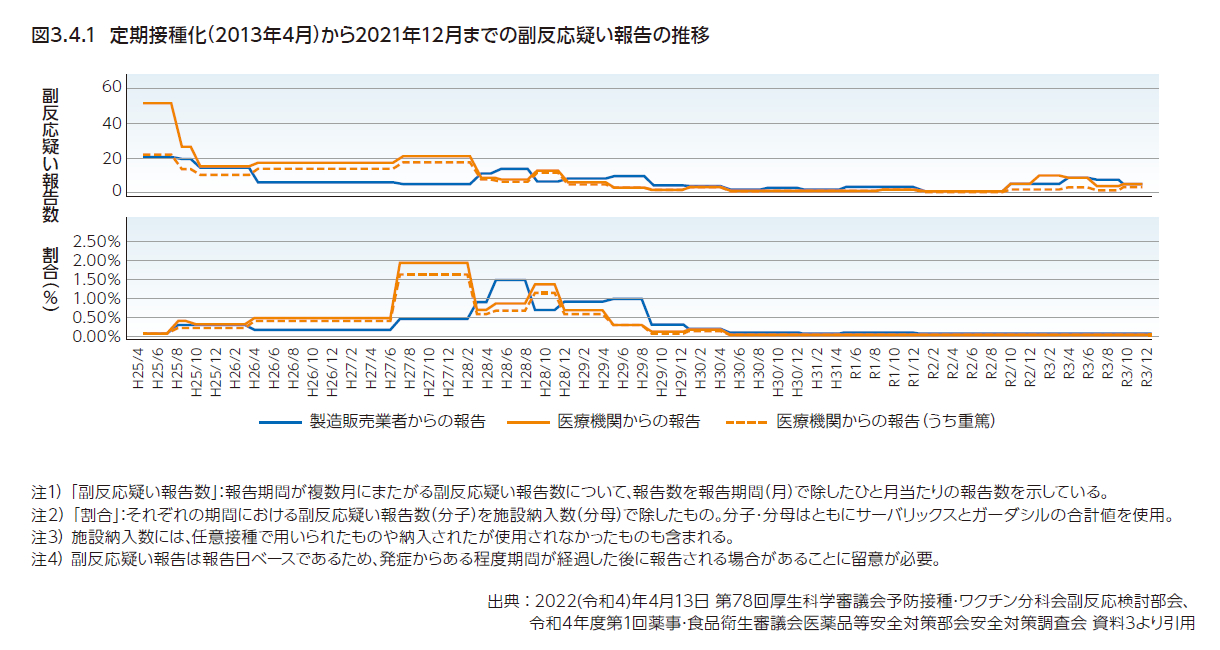
HPVワクチン接種は、子宮頸がんなどの原因となるHPV感染を予防するための重要な健康施策として導入された。しかしながら、市販承認後に副反応報告が増加し、2013年4月の定期接種化から2か月後に「積極的勧奨の差し控え」という措置がなされた(3.3参照)。この副反応には痛みのみならず、けいれんや健忘などの症状が出るとされ、ニュースや新聞などのマスコミで大きく報道された1–4)。この状況に伴い、HPVワクチンの接種率は激減し、問題がクローズアップされてから約2年後をピークに副反応疑い症例が多く報告された(図3.4.1)。
ワクチン接種後に見られた様々な症状
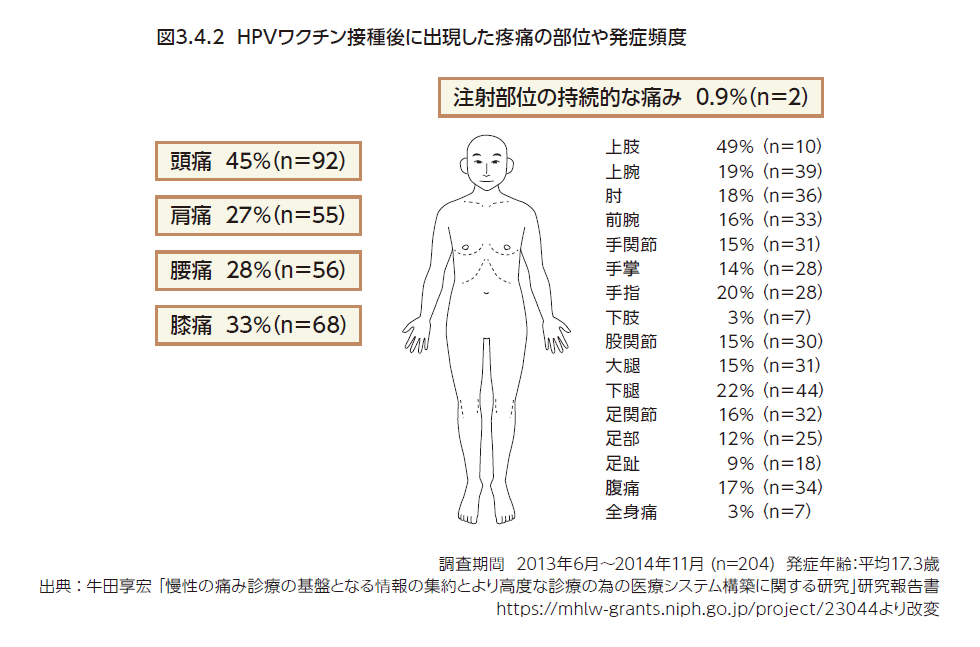
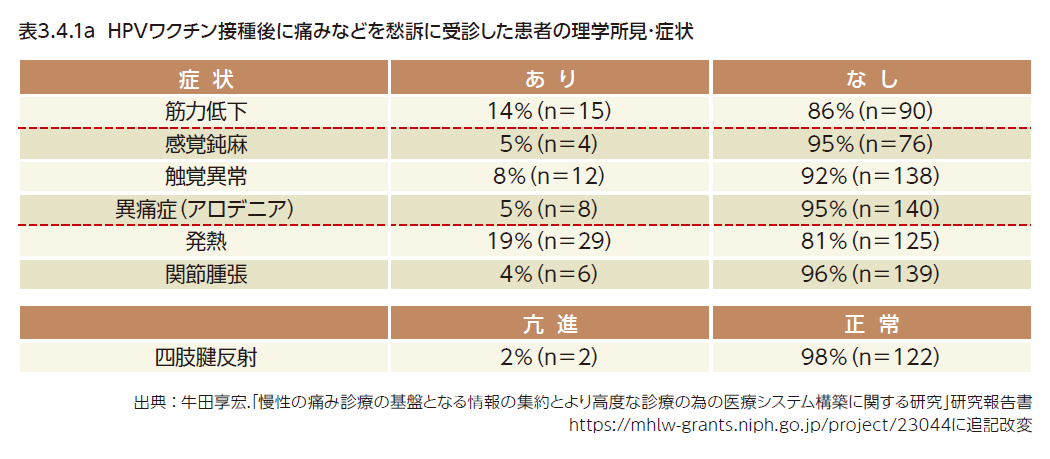
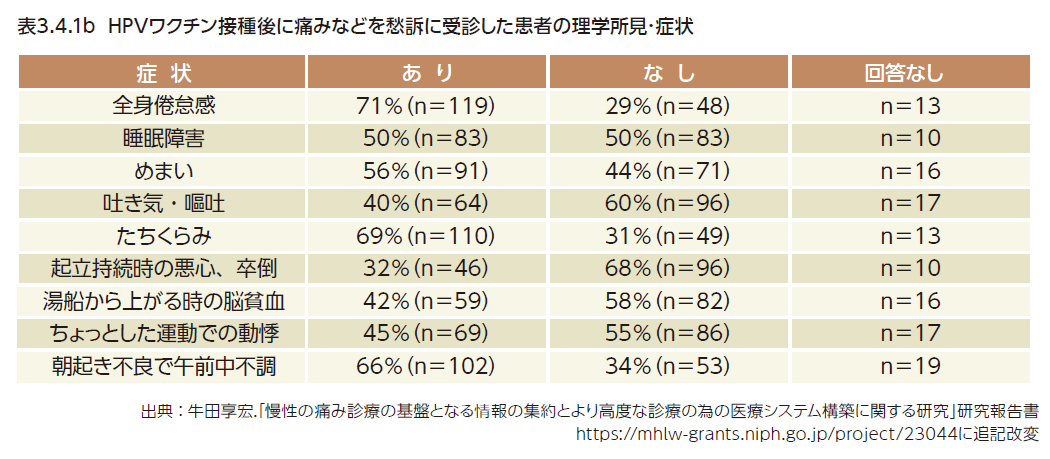
2013年~2014年度厚生労働科学研究費補助金慢性の痛み対策研究事業「慢性の痛み診療の基盤となる情報の集約とより高度な診療の為の医療システム構築に関する研究」(研究代表者:牛田享宏)では、ワクチン接種後に体調の不調を訴えた204名の患者の症状・所見を調査し(調査期間2013年6月~2014年11月)、疼痛や全身倦怠感、立ちくらみなどの機能性症状を訴えるものが多かったこと、一方で器質的な病態を示唆する身体所見や血液学的、症候学的な異常が診られるケースは少なかったことを報告している(図3.4.2、表3.4.1)5)。
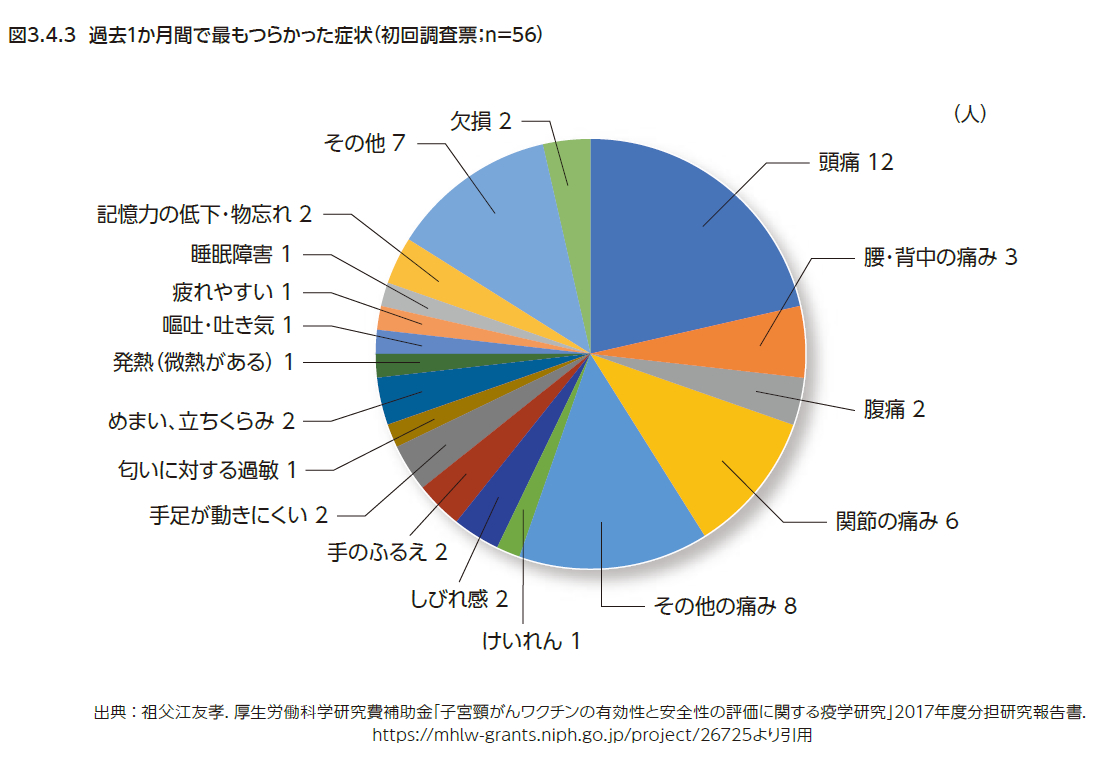
2015年~2017年度厚生労働科学研究費補助金「子宮頸がんワクチンの有効性と安全性の評価に関する疫学研究」(研究代表者:祖父江友孝)でも副反応疑いに関する追跡調査が行われ、全国の指定協力医療機関を通じて、HPVワクチン接種歴がありかつ組入れ基準(症例定義)を満たす患者とその家族に協力を依頼し、自記式質問紙票による調査を行っている。登録は56例(登録時の平均年齢:18.2歳)、直近のワクチン接種日から約4年が経過していた。症状出現時期は、直近のワクチン接種日から1ヵ月以内が37.5%、1年以内が76.8%であったが、発症日が不明の2例を含む約2割の患者はワクチン接種から1年後以降に症状が出現したとされる。「最もつらかった症状」の集計では、1位:頭痛、次いで、体幹や関節の痛み、めまい・立ちくらみ、手足の痺れ感、ふるえなどの症状が挙げられていたことが報告されている(図3.4.3)6)。
また、同研究班で別途実施された全国疫学調査によると、HPVワクチン接種後に生じたとされる症状と同様の「多様な症状」の推定有訴率は、男性では20(人口10万人対)、女性では40(人口10万人対)、HPVワクチン接種歴のない女性では20(人口10万人対)であり、接種歴の有無にかかわらず「多様な症状」を有する者が一定数存在するという結論であった6,7)。
引用文献
1)Ueda Y, Yagi A, Ikeda S, Enomoto T, Kimura T. Beyond resumption of the Japanese Government’s recommendation of the HPV vaccine. Lancet Oncol. 2018 Dec;19(12):1563-1564
2)Larson HJ. Japan’s HPV vaccine crisis: act now to avert cervical cancer cases and deaths. Lancet Public Health. 2020 Apr;5(4):e184-e185.
3)Tanaka Y. Time to resume active recommendation of the HPV vaccine in Japan. Lancet Oncol. 2020 Dec;21(12):1552-1553
4)Ikeda S, Ueda Y, Yagi A, Matsuzaki S, Kobayashi E, Kimura T, Miyagi E, Sekine M, Enomoto T, Kudoh K. HPV vaccination in Japan: what is happening in Japan? Expert Rev Vaccines. 2019 Apr;18(4):323-325.
5)牛田享宏.「慢性の痛み診療の基盤となる情報の集約とより高度な診療の為の医療システム構築に関する研究」研究報告書
https://mhlw-grants.niph.go.jp/project/23044,
(2023年2月9日アクセス)
6)祖父江友孝.厚生労働科学研究費補助金「子宮頸がんワクチンの有効性と安全性の評価に関する疫学研究」2017年度分担研究報告書.
https://mhlw-grants.niph.go.jp/project/26725,
(2023年2月6日アクセス)
7)Fukushima W, Hara M, Kitamura Y, et al. A Nationwide Epidemiological Survey of Adolescent Patients With Diverse Symptoms Similar to Those Following Human Papillomavirus Vaccination: Background Prevalence and Incidence for Considering Vaccine Safety in Japan. J Epidemiol. 2022;32(1):34-43.
3.4.2 HPVワクチン接種後に生じた症状に関する診療マニュアル
HPVワクチン接種後に身体の痛みなどの症状を訴えるケースがこれまでに報告されている(3.4.1参照)。特に定期接種の対象は思春期(小学校6年生~高校1年生相当)の女性のため、接種後に生じる可能性がある様々な症状の出現に対応するためには接種前、接種時、および接種後まで切れ目のないサポートが重要と考えられる。日本医師会・日本医学会では可及的な対応として2015年に有識者による「HPVワクチン接種後に生じた症状に対する診療の手引き」を発刊した1)。そこでは、基本的な診療姿勢、面接・問診のポイント、診察のポイント、検査、診断・鑑別診断、治療のポイントなど、その時点で有益性があり安全性が高いと考えられる対応などがとりまとめられた。その後、HPVワクチンの定期接種の積極的勧奨が再開されたのに併せて、厚生労働科学研究費補助金「HPVワクチンの安全性に関する研究」(研究代表者:岡部信彦)では2022年3月に「HPVワクチン接種後に生じた症状に関する診療マニュアル」を発出した2)。
この診療マニュアルは
- 多彩な症状:機能性身体症状、予防接種ストレス関連反応(ISRR)(3.2.3参照)や関連病態の理解
- HPVワクチン接種からフォローアップまでの流れ(ワクチンの接種時からのフロー、接種医の基本的な役割と診療姿勢、接種にあたる医師(接種医)やかかりつけ医の接種時と副反応出現時に果たすべき役割、予診票取得時の確認事項)
- 多様な症状の出現時に対応にあたる際の医師の診療姿勢と役割
- 副反応疑い出現時の書類などの対応と基準
- HPVワクチンに関するこれまでの経緯とエビデンス
- 予防接種・ワクチンの意義など
について詳述している。
ここでは、重要と考えられる①ファーストタッチ医(接種にあたる医師(接種医)やかかりつけ医)のワクチン接種前の対応、②副反応出現時の対応に当たる際のファーストタッチ医の診療姿勢と役割について当マニュアルの内容を紹介する(HPVワクチン接種後に生じた症状については3.4.1、診療体制については3.4.3をそれぞれ参照)。
① ファーストタッチ医のワクチン接種前の対応
不安や不信の状況はISRRなどの出現の素地となりえると考えられる。そのためファーストタッチ医は、ワクチンのメリットやISRRの出現も含めたデメリットについて保護者だけでなく接種される本人自身の納得と同意・署名を得た上でワクチン接種することが望ましい。接種前には「安心して接種していただくために、不安に感じることはありませんか」と必ず質問をし、接種される本人が「ない」と返事をしたとしても、不安そうな表情やそぶりが見受けられた場合や、当日に納得できていない様子がある場合は、強引に接種を勧めるのではなく、説明や確認のため接種日を改めるなどの対応が求められる。重大な既往があるなど接種が不適切と判断すれば中止するなどの柔軟な対応も考慮にいれる必要がある。
② 副反応出現時の対応に当たる際のファーストタッチ医の診療姿勢と役割
1. 面接・問診のポイント
-
真摯かつ優しい態度で、患者自身の話を中心に情報を整理する
本人が家族(親)の前ではしゃべりにくいケースがあることを念頭に置き”本人が親の前ではしゃべらない、親が本人の話を遮る、本人が親に視線を向けると親はそっぽを向く、本人が親の顔色を気にする、あるいは一切見ないなど”の様子についても留意し、必要に応じて記録する。 -
実際に何に困っているか、一日の生活内容を、時間をたどって詳細に聞く- どの部位に痛みが生じているのか
- 倦怠感はあるのか
- 運動障害はあるのか
- 記憶など認知機能の異常はあるのか
- そのほかの体調の変化などの症状はあるのかなどを聴取する。
「言えない(=言語化できない)」からこそ身体化症状が出ている子供(若者)がいることも念頭に置いて、状況を具体的に確認する。家族構成や学校など所属環境も確認する。身体面だけでなく生活面・心理・社会的な側面(食事、睡眠に関してどの程度確保できているのか?気分の落ち込みはあるか?社会参加の状況はどうか?)も可能な範囲で聞き取り検討する。
2. 診察のポイント
診察においては、全身を丁寧に診察し、本人と家族と診察所見を確認・共有することが原則である。
- 触診などによる理学所見を確認するこのことは病態の確認だけでなく医師-患者間の信頼関係の醸成にも繋がることから必須であり、診察毎に行うことが望ましい。痛みのある部位は、最初に触ると患者を不安・緊張させ、ほかの診察がしにくくなるため、最後に診察する。
- 筋力や運動障害の評価筋力低下や運動障害を訴える患者に対しては、徒手筋力テストで評価後に、患者の注意を筋力から逸らした方法で筋力を診ることによる所見の変動の有無の確認を行い、責任部位の推定の一助とする。徒手筋力テストで評価された筋力と、実際に歩行などの運動からの筋力評価の不一致があるかどうかを確認する。
- 客観的な下肢筋萎縮などのフォロー初診時には両側のCOT(膝蓋骨上10センチの大腿周囲径)、COLL(下腿最大周囲径)を計測し、後の脚の萎縮の進行の有無の目安とする。
- 臥位、座位での血圧測定(必要に応じ、立位での血圧の測定も検討する)
- 不随意運動のチェック振戦、ミオクローヌス、ジストニア、ジスキネジア、舞踏病様運動のいずれ該当するか、あるいは、組み合わさっているかを評価する。不随意運動では、驚愕反応に近い動きもありうる。
3. 検査(血液検査、画像検査など)
診断と除外診断のため、どんな疾患を疑い、どんな検査が必要かを十分に説明する。
- 緊急性のある疾患(炎症性、悪性など)については先に検査し、除外する必要に応じて、血液検査(スクリーニング)や尿検査、画像検査を検討する(リウマチ関連疾患などの除外も含めて)。
- 起立性調節障害に関する検査は、朝の体調不良などがある場合に検討する
- 身体局所の異常所見があれば、その異常に応じた診療科の専門医の診察と意見を求めることを検討する(例:筋萎縮がある→整形外科医や神経内科医/小児神経医、不随意運動→神経内科医/小児神経医、皮膚の色調変化→皮膚科/麻酔科医)
4. 鑑別診断
1)痛みの一般的鑑別
- 頭痛:片頭痛、筋緊張性頭痛、顎関節症、起立性調節障害など
- 頚部痛:頚椎疾患、姿勢異常など
- 手足のしびれ痛み:神経障害性疼痛(末梢神経や神経系による痛み)神経内科疾患
- 関節痛・筋痛:炎症性関節疾患(関節リウマチ、膠原病など)、膝内障など関節拘縮・関節弛緩およびこれらに伴う腱付着部炎
2)その他の痛みを伴う稀な疾患
思春期を中心とする対象年齢では、代謝疾患、悪性新生物、肢端紅痛症、レイノー病、成長痛、慢性反復性多発骨髄炎、ビタミンD欠乏症、甲状腺機能亢進・低下症などがあるが、頻度は少ないため地域の医療機関で全ての患者に検査を行うのではなく、これらを疑う場合に、協力医療機関や専門医療機関に紹介することを検討する。
3)麻痺や運動異常
- 脳・脊髄関連疾患:てんかん、ニューロパチー疾患、脊髄症・ミエロパチー、神経傷害によるもの
- 非てんかん発作
5. 診断の考え方とその伝え方
- 単回の診察での断定的な診断や患者・家族への告知は基本的に避ける。
- 患者の訴える症状とその経過、診察所見、検査所見、ほかの専門医の意見、心理社会的要因からの修飾を総合的に考え、「患者が訴える多様な身体症状とその経過が、一般的身体疾患や物質の直接的作用、注射行為によって説明可能かどうか」を判断する。
- 特に患者・家族は早期の診断を希望すると思われるが、Red Flag(重大な器質的疾患)やその他の疾患(膠原病や運動器疾患など)がないことを比較的早期に判断する必要がある一方で、それがなければ、不安にさせず時間をかけながら関係性を構築する。
- 病態の説明が難しい場合や病態が一つの原因では説明困難と判断する場合には、病名を付けることに固執せず、何回か受診した段階(一般的には1か月程度)で器質的な重篤な病気ではないことを説明する。その際、症状や不安が強くないケースについては、接種時の体調など様々な要因が関連して多様な症状が生じたりすることがあるが、対症療法で、症状の改善が期待できることが多いことを説明する。また、症状が強くみられ不安が強い場合には、患者・家族に寄り添って安心して治療を行うことができる環境を作るように心がけ、体力の維持をはかりつつ、根拠のない医療などへの依存を含めた不適切な行動を行わないような説明・指導を行う。寄り添う例としては、「症状が非常に苦しいのはわかるが、今の医学では明確な原因はみつからない。必要な診察や検査は終わって、治療しなければ命に関わるような病変がないことは間違いなく言える。今後、何か体の異常がでてくる可能性や、こういう体の症状が環境のストレスなどによって起こることもあることを考えて、しばらく通って、経過をみせてほしい。その間に必要な検査などあればするようにしたい。」など、関係性を大切にした診療対応を行う。どのような場合でも、病態は変化しうるものと考えるべきであり、経時的にフォローするあるいは常に来院し相談できる医療環境の構築に努める。
6. 治療のポイント
ファーストタッチ医においては以下について留意し、必要であれば協力医療機関としっかりと連携しつつ診療をすすめる。
- Red Flagなどを含めて、明確な器質的疾患と診断された場合は、先に述べたような関係性を保ちつつ、専門医での治療の流れに導く。
- CRPS(複合性局所疼痛症候群など)や線維筋痛症などの疼痛疾患が疑われた場合は、自分の専門でないと説明して慢性疼痛を専門にしている協力医療機関での治療に導く。
- それ以外のケースにおいては認知行動療法的治療やリハビリテーションを基本とし、必要性がある場合には安全な範囲内での薬物療法を考慮する。なお、薬物療法を行う際にはよくなる可能性、症状が変わらない可能性など十分説明した上で行う。
- 治療は身体を以前の状態に戻すことではなく、成長過程も含めて新たな心身の状態に変わっていくことで適応していくというプロセスであるということを共有しながら進めていく必要がある。従って、治療目標は生活内容の改善が第一であり、症状は移りゆくものであって、問題とすることなく本人の希望する生活ができるようになることを患者とも共有し支援する。
1) 患者・家族・医療者の疾患認識の共有
患者、家族に対して病態や治療方針について繰り返し説明を行い、理解を得ることで不安などによる心理社会的リスクの軽減を図る。
- 神経系の変調によって起きた痛みであり運動は可能なこと(「打撲などの痛みでは鎮痛剤が効くのにこの痛みには効かない」と患者は区別する)
- 本人のせいではないこと
- 運動などにより筋力・運動能力を付けていくとたとえ痛みがあっても困らず生活はできるようになるものであること
2) 認知行動療法的治療
- 客観的事実を共有し、不安というだけで行動を抑制しないよう促す
- 痛む体を動かしても体自体は悪くならないことを繰り返し説明する
- 痛みの消失ではなく、生活が可能な、痛みが30〜40%に低減することを目標とする
- 緊張を和らげ、痛みをやりくりするための方法を自ら探すよう手助けする
- 発症以前にできたことだけでなく、新たにやりたいことも目標、課題とする
3) リハビリテーション
- 思春期が将来に向けての筋・骨を成長させる(蓄える)重要な時期であることを説明した上で、日常的に可能な運動を積極的に勧めることを基本とする
- 痛みによって廃用になり、関節の拘縮や筋の委縮など器質的異常が起きる可能性があれば、リハビリテーション専門施設に依頼して積極的に治療介入を検討する
- 運動による痛みの増強があっても、患者が自己身体に対する自信を回復できるよう支援し、辛抱強くリハビリを継続することを推奨する
- このような治療法では、少なくとも1か月以上は継続することが重要であることを教育する
- 病初期には、日常的な運動を制限しない、可能な運動を勧めるなどして、杖や車椅子、コルセットなどの補助器具の使用を避けることが重要で、組織傷害が明確でない場合には安易に安静を指導しないようにする
4) 薬物療法
- 鎮痛薬
小児への薬剤投与にあたっては問題点が大きく3つある。1つ目は保険適応の有無、2つ目は投与量、3つ目は投与方法である。基本的に鎮痛薬を常用するケースはまれであるため、小児用量の記載がある薬は非常に少ない。さらに、錠剤を内服できなかったり、味や舌触りなどの理由で散剤が飲めなかったりする子どももいる。安全性も加味すると、アセトアミノフェンとイブプロフェンが選択される。炎症反応を抑えるときには、小児に使用できる数少ないNSAIDs(非ステロイド性抗炎症薬)であるイブプロフェンを選択する。無効な場合や副作用が強く出ることがあるため、選択と用法には工夫が必要である。 - 睡眠薬、筋弛緩剤など
ベンゾジアゼピン系の薬剤は依存性の観点から使用しないことを基本とする。
5) その他の症状に対する対症療法
- 易疲労感や睡眠障害
体内時計を環境に合わせるため、朝夕の自然な日照に合わせて基本的生活を守るよう指示しながら、できるだけ自発性を尊重して無理をしない。体力を回復させるためにも覚醒時痛みが落ち着いている時間帯に運動や活動を推奨する。睡眠障害に対しては、症状を詳細に把握し、日中の機能障害を確認する。睡眠衛生指導をおこなうことで改善がみられることが多い。寝る直前のスマートフォンやタブレットの使用は体内時計を遅らせるため、使用時間の確認をする。不眠時、睡眠導入薬については安易な使用は避ける。 - 非てんかん性発作
全身性のけいれん様のものからミオクローヌス様のものまで多様なものが見られるが、全例に共通した特定のパターンを持つ脳波異常は確認されていない。全身性の運動器症状を呈している場合にはリカバリーポジションなど安全な姿勢をとらせ、できるだけ刺激せずに観察する。視覚や聴覚は遮断されていないことが多く、痙攣発作や過呼吸など危険な状態にならなければ、薬物治療は避ける。なお、繰り返し発作が起こる際には専門医と連携し、評価を行なった上で対応方法について検討を行う。
引用文献
1)公益社団法人 日本医師会/日本医学会.HPVワクチン接種後に生じた症状に対する診療の手引き.2015.
https://www.mhlw.go.jp/bunya/kenkou/kekkaku-kansenshou28/dl/yobou150819-2.pdf,
(2022年11月15日アクセス)
2)一般財団法人日本いたみ財団.「HPV ワクチン接種後に生じた症状に関する診療マニュアル」.
https://nippon-itami.org/hpv-vaccine_form,
(2022年11月15日アクセス)
中村有里.「年代別注意すべき患者特性 小児」運動器慢性痛治療薬の選択と使用法.南江堂.194-196,2015
3.4.3 相談支援・医療体制
厚生労働省は、HPVワクチン接種後に痛みなどの様々な症状がみられた人が地域において相談や適切な診療を受けることができるために、診療・相談体制および報告・救済制度を国、都道府県および市町村および協力医療機関を中心に構築している1)。
① 診療・相談体制
1. 面接・問診のポイント
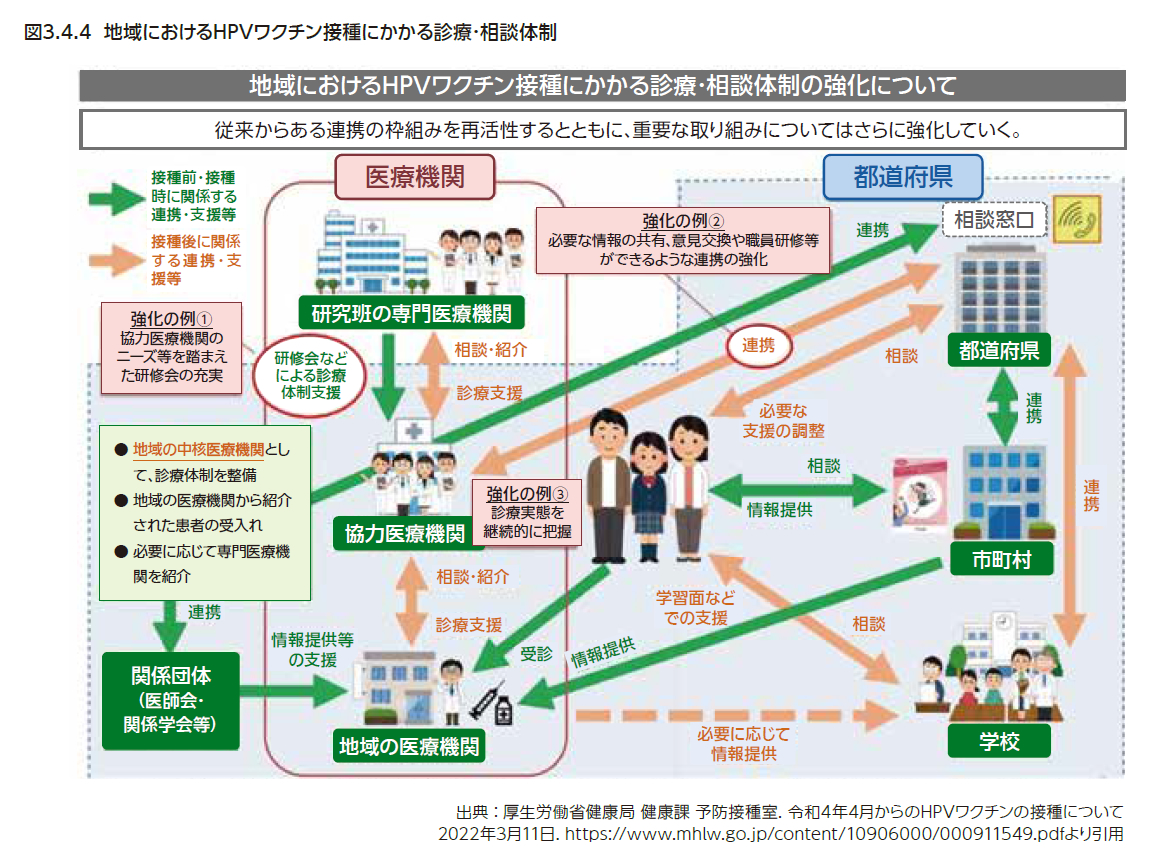
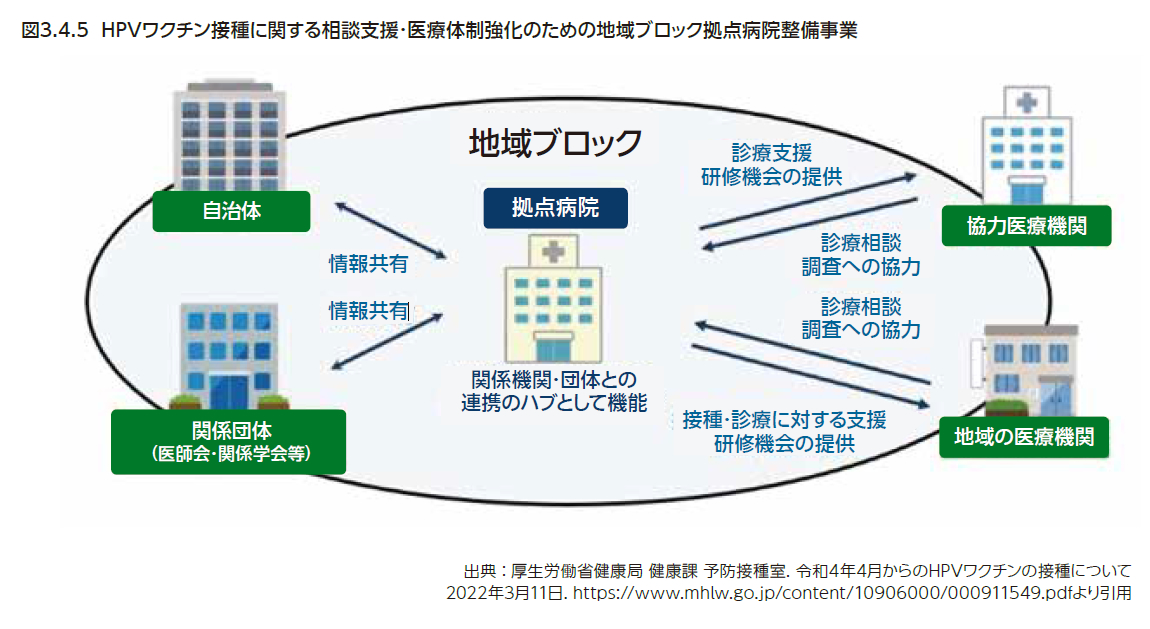
図3.4.4に地域におけるHPVワクチン接種にかかる診療・相談体制の枠組みを示す。多様な症状に対する診療体制は、2013年9月から厚生労働省科学研究費補助金の研究班に所属する医師の医療機関が中心となって整備が進められてきた2)。その後、より身近な地域で受診できるように、2014年9月の厚生労働省通知に基づいて3)、各都道府県に協力医療機関が選定された。2022年3月7日現在、47都道府県83医療機関が選定されている1)。さらに、2022年4月から厚生労働省はHPVワクチンの積極的勧奨の再開に伴い、拠点病院事業を開始した。ワクチン接種後に痛みなどの症状を引き起こす患者を診療するためのチーム医療体制の構築と、自治体、医師会、協力医療機関ならびに厚生労働科学研究費補助金の研究班の連携・教育研修、情報共有のハブとしての働きを、全国8ブロックでそれぞれ指定した拠点病院にもたせるものである(図3.4.5)。2022年11月現在、9つの医療機関が拠点病院として指定されている4)。今後、拠点病院間での情報共有や厚生労働研究班との協力などを進めることで、多様な症状の全国の発生状況を逐次モニタリングしながら連携して診療し、安全にワクチン接種が進められることを目指すものである。
2. ファーストタッチ医と協力医療機関の役割
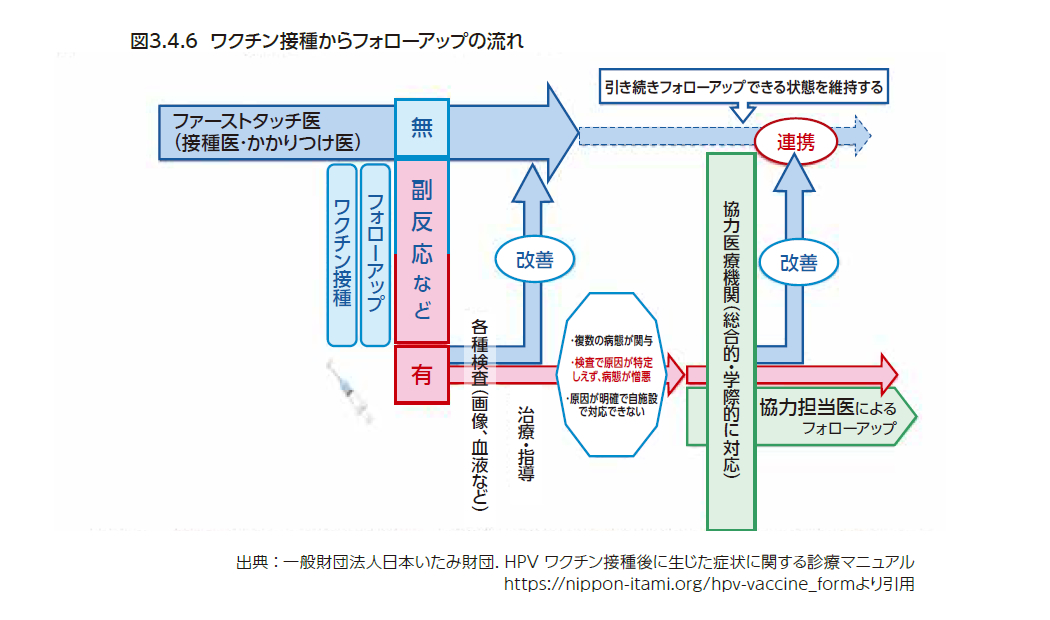
HPVワクチン接種後の痛みなどの多様な症状の治療にあたっては患者が「たらい回し」になることがないような連携体制の構築が最も重要である。特に最初に診療にあたった医師(接種医などが望ましい)はファーストタッチ医として患者および家族との関係性を構築しつつ、診療に当たり副反応などの状況チェックや初期対応を行う。また、症状発症に複数の病態が関与している場合、原因がわかっていても自施設で対応できない場合、症状が増悪してきているにもかかわらず原因が明確にできない場合にファーストタッチ医は必要に応じて各都道府県が定めた協力医療機関と連携して診療にあたる(図3.4.6)。
② 報告・救済制度
1. 副反応疑い報告制度
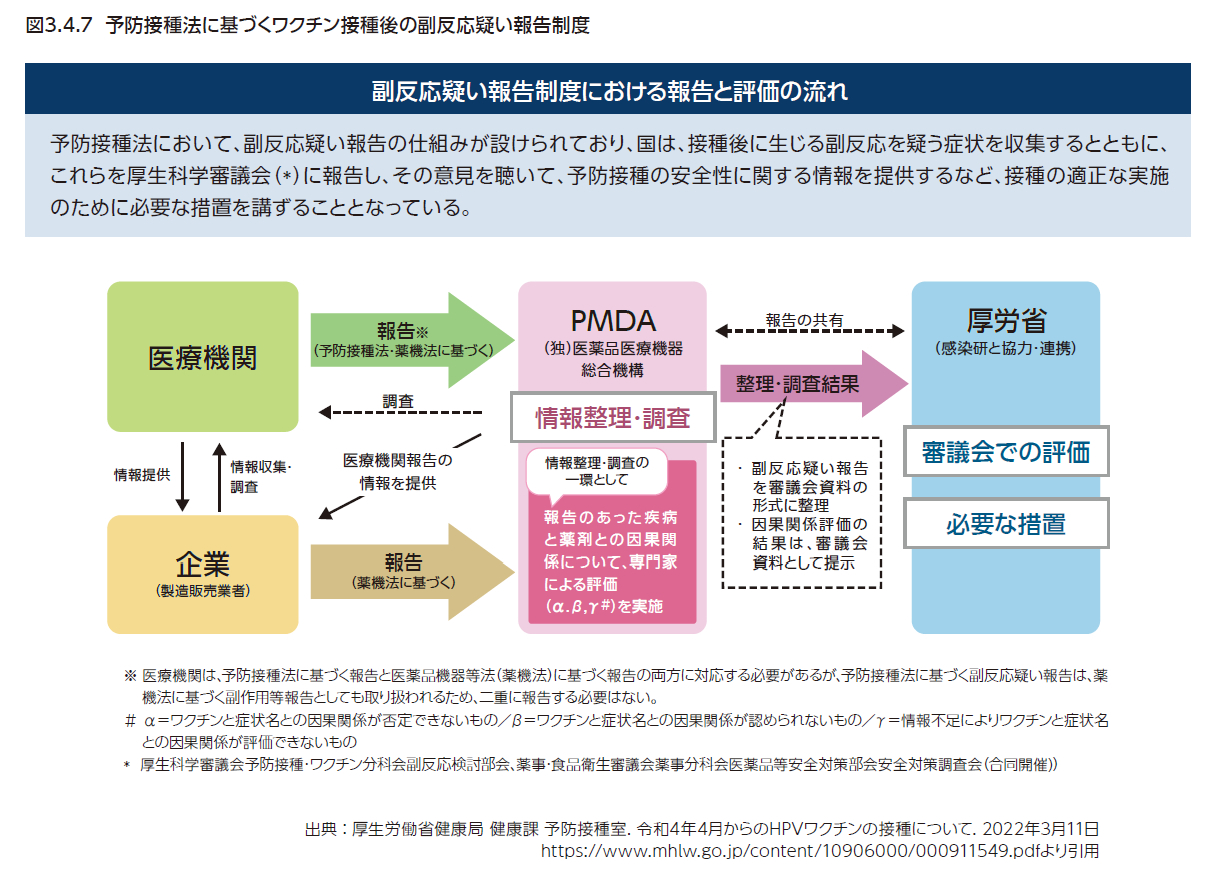
図3.4.7に予防接種法に基づくワクチン接種後の副反応疑い症例の報告制度を示す。医療機関は、副反応疑い症例を所定の書式で独立行政法人医薬品医療機器総合機構(PMDA)に報告する。2021年度より従来のFAXに加えて電子報告システムでの報告が可能となっている5)。PMDAでは、報告のあった疾病と薬剤との因果関係について、専門家による評価を含む情報の整理・調査結果を提示し、厚生労働省は、厚生労働科学審議会による評価に基づいて必要な措置を講ずる。
2. 相談支援体制と救済制度
1) 国の相談窓口
厚生労働省感染症・予防接種相談窓口では、HPVワクチンを含む予防接種、インフルエンザ、性感染症、その他感染症全般についての相談を受け付けている。
厚生労働省 感染症・予防接種相談窓口
https://www.mhlw.go.jp/bunya/kenkou/kekkaku-kansenshou01/inful_consult.html
2) 都道府県の相談窓口
各都道府県では、どこに相談すればよいか分からない、診察してくれる医療機関を紹介してほしい(衛生部門担当窓口)、学校生活に関する相談をしたいなど、HPVワクチンの接種前、接種後の多様な相談に対応できる窓口を設けている。
東京都の例:HPVワクチンの定期予防接種について(東京都福祉保健局)
https://www.fukushihoken.metro.tokyo.lg.jp/iryo/kansen/hpv.html
3) 市町村の相談窓口
各市町村の予防接種担当課(健康増進課や健康福祉課など)が相談を行っている。
市町村のホームページに情報が掲載されている。
4) 救済制度
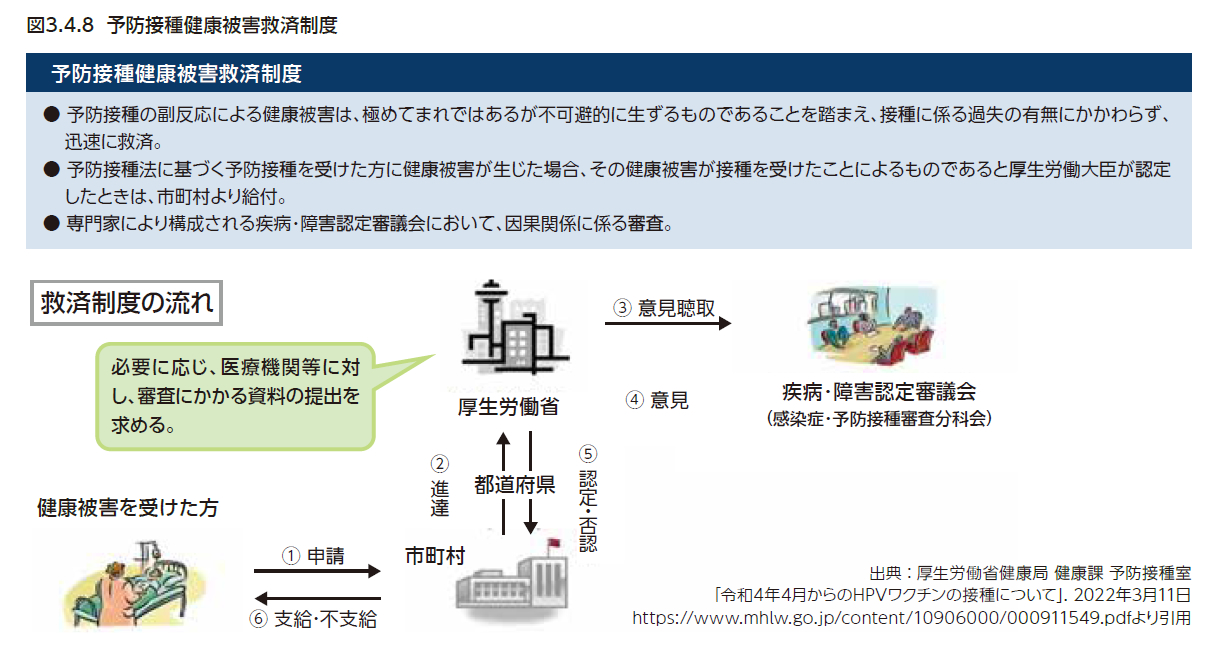
図3.4.8に予防接種の健康被害の救済制度の枠組みを示す。予防接種法に基づく予防接種(定期接種)を受けた人に健康被害が生じた場合、被害を受けた人の市町村への申請に基づいて、因果関係の審査を行い、その健康被害が接種を受けたことによるものであると厚生労働大臣が認定したときは、市町村より救済、医療費などが給付される。2013年度以降定期接種を受けた人については、予防接種法に基づく救済が適用され、医療費の救済範囲が入院相当に限定されなくなった(それまでのPMDA法に基づく救済では「通院は入院相当」とされていた)。救済制度の詳細や申請方法は厚生労働省のウェブサイトに記載されている6)。各市町村の予防接種担当課が直接の窓口になるほか、PMDAにも相談窓口がある。独立行政法人医薬品医療機器総合機構(PMDA)救済制度相談窓口
https://www.pmda.go.jp/relief-services/adr-sufferers/0020.html
引用文献
1)厚生労働省健康局健康課予防接種室.「令和4年4月からのHPVワクチンの接種について」.
https://www.mhlw.go.jp/content/10906000/000911549.pdf,
(2023年2月10日アクセス)
2)公益社団法人 日本医師会/日本医学会.HPVワクチン接種後に生じた症状に対する診療の手引き.2015年
https://www.mhlw.go.jp/bunya/kenkou/kekkaku-kansenshou28/dl/yobou150819-2.pdf,
(2023年2月10日アクセス)
3)厚生労働省健康局結核感染症課長.ヒトパピローマウイルス感染症の予防接種後に生じた症状の診療に係る協力医療機関の選定について.
https://www.mhlw.go.jp/bunya/kenkou/kekkaku-kansenshou20/dl/yobou140929-1.pdf,
(2023年2月10日アクセス)
4)厚生労働省健康局健康課予防接種室.ヒトパピローマウイルス感染症の予防接種に関する相談支援・医療体制強化のための地域ブロック拠点病院整備事業の実施機関の決定について.
https://www.mhlw.go.jp/content/000924325.pdf,
(2023年2月10日アクセス)
5)独立行政法人 医薬品医療機器総合機構.「報告受付サイト」.
https://www.pmda.go.jp/safety/reports/hcp/0002.html,
(2023年2月10日アクセス)
6)厚生労働省.「予防接種健康被害救済制度について」.
https://www.mhlw.go.jp/stf/seisakunitsuite/bunya/vaccine_kenkouhigaikyuusai.html,
(2023年2月10日アクセス)
3.5 諸外国におけるHPVワクチンプログラムと接種率向上対策
① 子宮頸がん撲滅のための世界戦略
2020年8月、世界保健機関(WHO)は子宮頸がんの撲滅のための世界戦略および関連する目標とターゲットを採択した。その戦略の中で、WHOは各国が子宮頸がんの罹患率を4(人口10万対)未満に下げるために、1)HPVワクチン、2)がん検診、3)治療とケア、の3つ分野で2030年までに達成すべき目標を掲げている1)(表3.5.1)。
② 諸外国におけるHPVワクチンプログラムと接種率
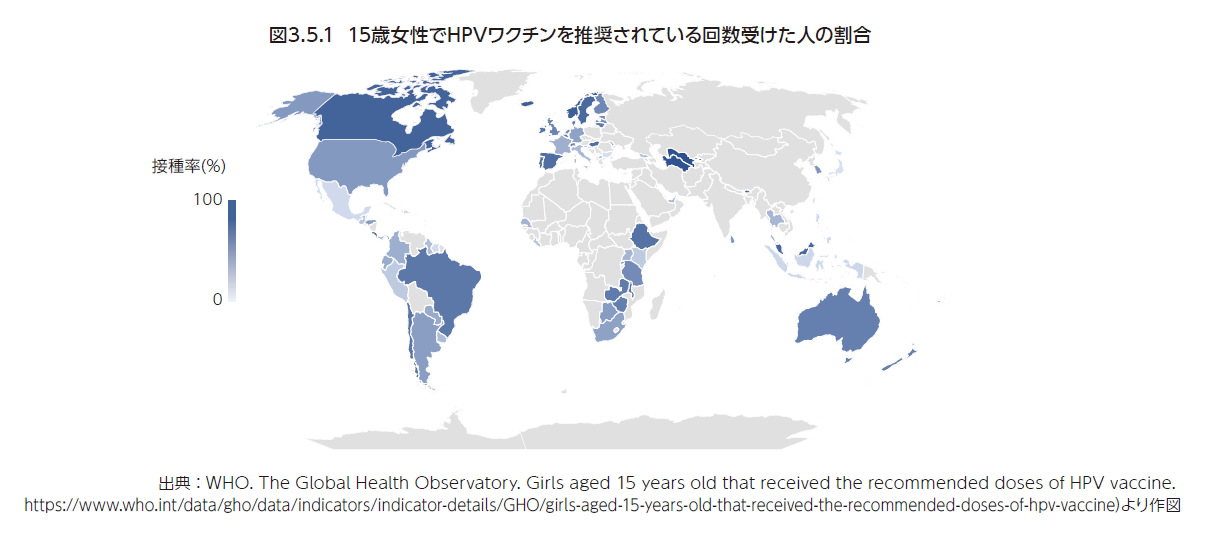
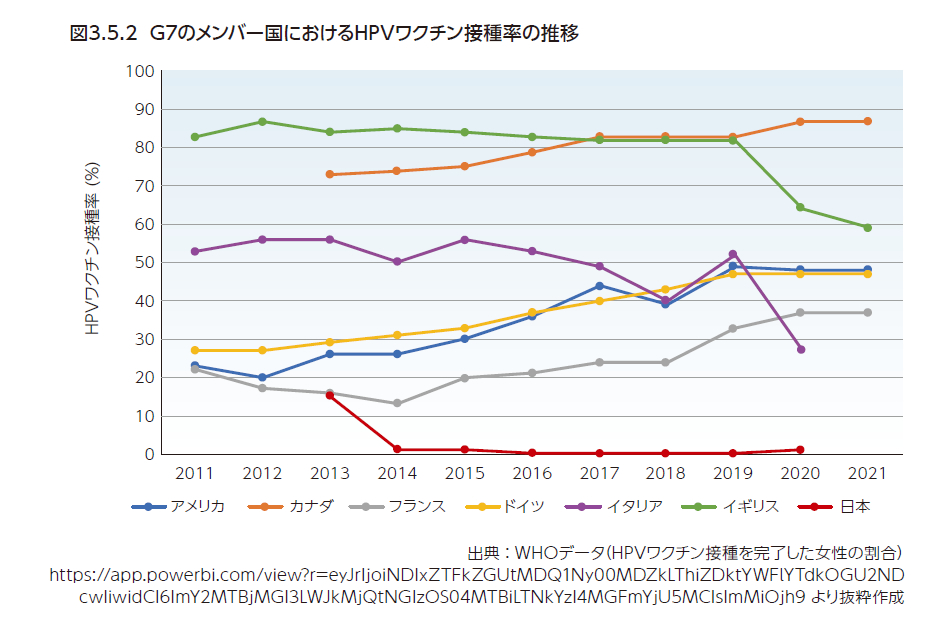
1番目の目標であるHPVワクチン接種の取り組みとして、HPVワクチンを国の予防接種プログラムに取り入れる国が年々増加しており、その数は2022年11月24日時点のデータによると124か国に達している2)。しかしながら、世界のHPVワクチン接種率は15歳以下の女性で44%であり2)、WHOが掲げている90%を大きく下回っている。2022年11月のデータによると、90%接種率を達成している国はウズベキスタン、トルクメニスタン、アイスランド、ノルウェーのみで(図3.5.1)、HPVワクチンが国の予防接種プログラムに導入されている国の半数近くで50%を下回っている3)。特に日本では、2013年の積極的勧奨の差し控え後に接種率が著しく下がり(3.3参照)、ほかのG7の国々をはじめとする多くの国に大幅に遅れをとっている(図3.5.2)。
WHOはHPVワクチン接種回数について、1回または2回(21歳以上においては2回、免疫抑制状態にある者は2回あるいは3回)を推奨している4)(3.2参照)。日本を含む3か国は3回接種を主体としているが(2023年2月時点)、大半の国は主な対象集団に対して2回接種を実施している。オーストラリアでは2023年2月6日からキャッチアップ接種対象者を含め、2回接種から1回接種へと移行した5)。
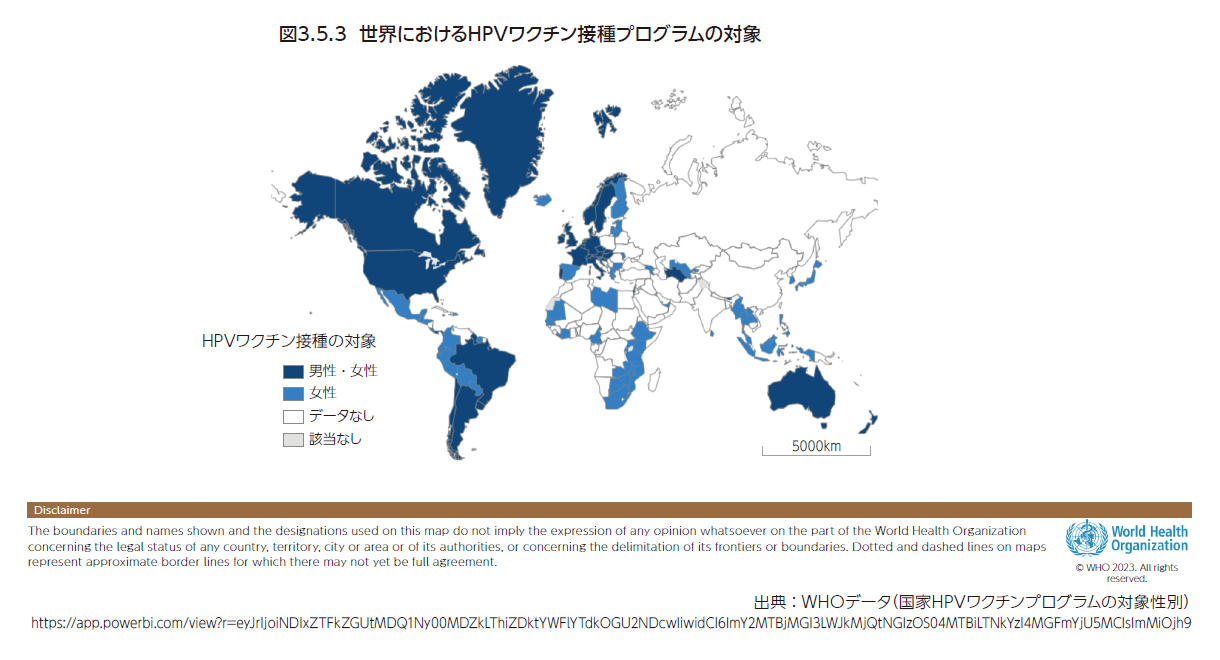
HPVワクチン接種対象については、アメリカ、オーストラリア、カナダ、ノルウェーなど、117か国中39か国(2023年2月時点)で、男性も国家HPVワクチンプログラムの対象に含めている(図3.5.3)。
③ HPVワクチン接種率向上のための対策
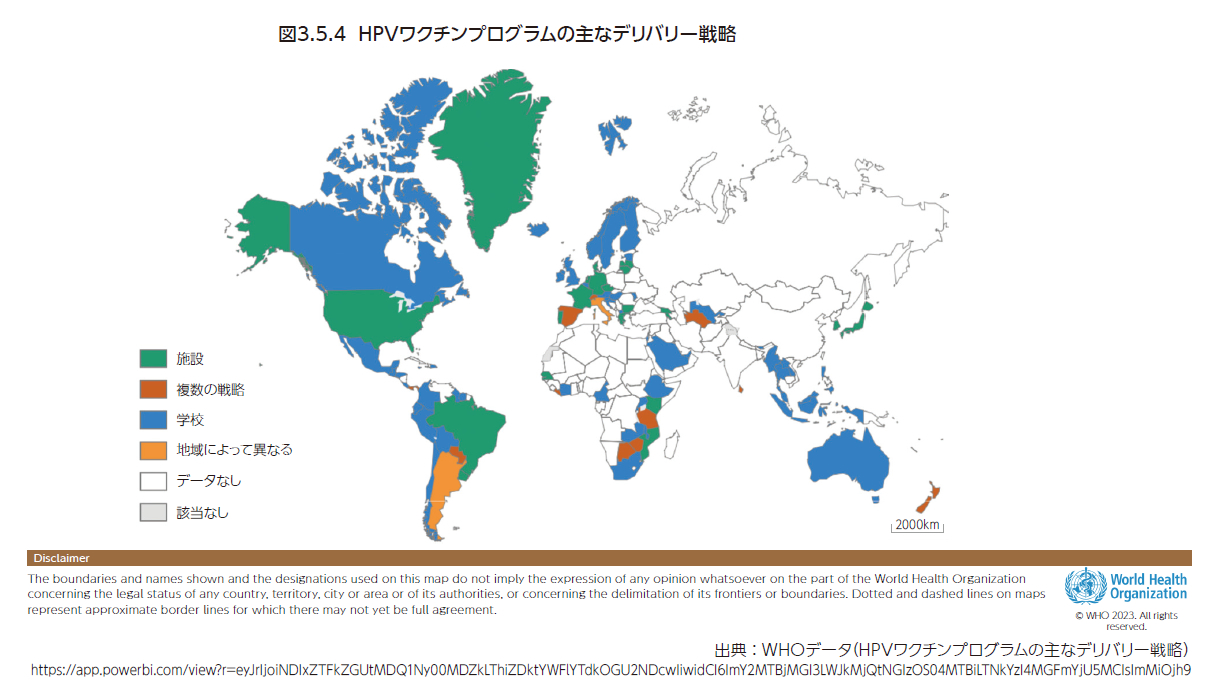
米国のCommunity Preventive Services Task Force(CPSTF)は予防接種率を高めるための対策として、予防接種へのアクセスの改善や地域社会の予防接種意欲の向上を目的とした介入方法を推奨している6)。例えば、予防接種へのアクセスを改善させるための介入として、学校や児童センターで実施する予防接種プログラムを推奨している。そのプログラムには予防接種の実施だけではなく、予防接種に関する教育、予防接種状況の確認と追跡、予防接種を受けていない子供の予防接種提供者への紹介といった内容が含まれる。2023年2月7日時点のWHOのデータによると、学校でHPVワクチン接種を行っている国は世界で68か国ある(図3.5.4)。欧州では、HPVワクチン接種が学校で実施されている国でHPVワクチン接種率が高いという報告もある7)。ほかにも、予防接種へのアクセスを改善させるための介入として、地域団体、自治体、予防接種提供者が連携し、女性、乳児、小児が訪れる医療環境におけるアクセスの拡大、自宅訪問、自己負担額の削減などを推奨している7)。地域社会におけるワクチン接種への意欲を高める対策としては、リマインダー(ワクチン接種予定日前)・リコール(ワクチン接種予定日後)、被接種者あるいはその家族への報酬(ギフト券、ベビー用品など)、アウトリーチと追跡、ワクチン接種対象者または地域社会全体の教育などの対策を組み合わせて実施することが推奨されている。
さらに、CPSTFは医療体制への介入として、予防接種情報システム(immunization information systems:IIS)を推奨している8)。IISは、ある地域に居住する人々に対して、参加医療機関が行ったすべての予防接種を記録するデータベースで、リマインダー・リコール、医療提供者の評価とフィードバック、それから臨床医、保健所、学校による予防接種状況の把握が可能な仕組みである。こうしたシステムは接種率の把握、無効な接種の回避、ワクチン接種率の格差に関する評価への情報提供、そしてワクチン供給に関する管理および説明責任を促進する上で役立つ。ほかには、医療従事者へのリマインダーやスタンディング・オーダーが接種率向上のための介入方法として推奨されている6)。スタンディング・オーダーは、看護師、薬剤師、および法で認められているその他の医療提供者に、施設、医師、またはその他の認可された提供者が承認したプロトコルに従って、予防接種を実施する権限を与えるものである。
HPVワクチン接種率を上げるために、以上に述べたような科学的根拠に基づいた方策を、わが国の文化・社会的背景、保健医療制度、実現可能性、持続性などを考慮した上で実行することが重要である。
引用文献
1)World Health Organization. Global strategy to accelerate the elimination of cervical cancer as a public health problem. Geneva: World Health Organization; 2020. Licence: CC BY-NC-SA 3.0 IGO.
https://www.who.int/initiatives/cervical-cancer-elimination-initiative
2)World Health Organization.「HPV vaccine included in national immunization programe」.
https://app.powerbi.com/view?r=eyJrIjoiNDIxZTFkZGUtMDQ1Ny00MDZkLThiZDktYWFlYTdkOGU2NDcwIiwidCI6ImY2MTBjMGI3LWJkMjQtNGIzOS04MTBiLTNkYzI4MGFmYjU5MCIsImMiOjh9,
(2022年11月24日アクセス)
3)World Health Organization.「The Global Health Observatory. Girls aged 15 years old that received the recommended doses of HPV vaccine」.
https://www.who.int/data/gho/data/indicators/indicator-details/GHO/girls-aged-15-years-old-that-received-the-recommended-doses-of-hpv-vaccine,
(2022年12月5日アクセス)
4)World Health Organization. Human papillomavirus vaccines: WHO position paper, December 2022. Weekly Epidemiological Record No 50, 2022, 97, 645–672.
https://www.who.int/publications/i/item/who-wer9750-645-672,
(2023年2月20日アクセス)
5)Department of Health and Aged Care.「Change to single dose HPV vaccine」. 2023年2月6日.
https://www.health.gov.au/ministers/the-hon-mark-butler-mp/media/change-to-single-dose-hpv-vaccine?language=en,
(2022年2月7日アクセス)
6)The Community Guide.「CPSTF Findings for Increasing Vaccination」. 2019年8月27日.
https://www.thecommunityguide.org/pages/task-force-findings-increasing-vaccination.html#increasing-demand,
(2022年12月5日アクセス)
7)Nguyen-Huu NH, Thilly N, Derrough T, et al. Human papillomavirus vaccination coverage, policies, and practical implementation across Europe. Vaccine. 2020;38(6):1315-1331.
8)Community Preventive Services Task Force. Increasing Appropriate Vaccination: Immunization Information Systems.
https://www.thecommunityguide.org/media/pdf/Vaccination-Immunization-Info-Systems.pdf,
(2022年2月7日アクセス)
[ad_2]
Source link